Trophoblast Funksjoner, lag og utvikling
den trophoblast er en struktur utgjøres av et sett av celler som danner det ytre laget som omgir en blastocyst, i tidlige stadier av den embryonale utviklingen av pattedyr. Begrepet kommer fra gresk trofos, som betyr "feed"; og av jeg blast, som refererer til den embryonale bakteriecellen.
Under de tidlige stadier av graviditet av plasentale pattedyr, er trofoblastcellene de første som skiller seg inn i en eggløsning som er befruktet. Dette settet av celler er kjent som trofoblast, men etter gastrulasjon kalles de trophoectoderm.
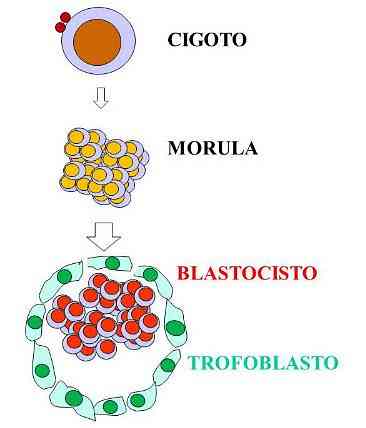
Trofoblast gir næringsverdige molekyler til det utviklende embryo og letter implantasjonen til livmorveggen på grunn av sin evne til å ødelegge livmorens liv. Blastocysten kan således forbinde kaviteten dannet av livmorveggen, hvor den vil absorbere næringsstoffene fra væsken som kommer fra moren.
index
- 1 Funksjoner
- 2 lag
- 2.1 Sincitiotrophoblast
- 2,2 Citotrophoblast
- 3 Utvikling
- 4 referanser
funksjoner
Trofoblast spiller en avgjørende rolle i implantasjon og placentasjon. Begge prosessene oppstår riktig som følge av molekylær kommunikasjon mellom føtal og maternelt vev, formidlet av hormoner og membranreseptorer.
Under implanteringen av blastocysten genereres nye typer forskjellige trofoblastiske celler, kalt villøs og ekstravilløs trofoblast. Den første deltar i utvekslingen mellom fosteret og moren, og sistnevnte knytter legemet til livmorveggen.
På den annen side er placentasjonen preget av invasjonen av livmorhalsspiralene ved ekstravellosus trofoblastiske celler som oppstår ved forankringen av villi. På grunn av denne invasjonen erstattes den arterielle strukturen med amorffibrinoidmateriale og endovaskulære trofoblastiske celler..
Denne transformasjonen etablerer et perfusjonssystem med lav kapasitet og høy kapasitet fra de radiale arteriene til det mellomliggende rom, hvor det hårete treet er innebygd.
Graviditetens fysiologi er avhengig av den ordnede utviklingen av strukturelle og funksjonelle endringer av villøs og ekstravilløs trofoblast.
Dette betyr at en forstyrrelse av slike prosesser kan føre til forskjellige typer komplikasjoner av varierende grad av alvorlighetsgrad, inkludert mulig tap av graviditet og dødelige sykdommer.
Trofoblasten, selv om den ikke direkte bidrar til dannelsen av embryoet, er en forløper av moderkaken, hvis funksjon er å etablere en forbindelse med mors livmoder for å tillate ernæringen til det utviklende embryo. Trofoblast er tydelig fra dag 6 i humane embryoer.
lagene
Under implantasjonen vokser trofoblastmultiplikasjonene og skilles i to lag:
sincitiotrofoblasto
Syncytiotrophoblast er det ytre laget av trofoblast, dets celler har ikke intercellulære grenser fordi deres membraner har gått tapt (syncytium). Av denne grunn observeres cellene som multinukleert og danner ledninger som infiltrerer endometriumet..
Cellene i syncytiotrophoblast kommer fra fusjonen av cellene i cytotrofoblastet, og deres vekst fører til dannelsen av chorioniske villi. Disse tjener til å øke overflaten som tillater strømmen av næringsstoffer fra mor til foster.
Gjennom apoptose (programmert celledød) av livmorstromcellene blir det opprettet rom hvor blastocysten trenger inn i endometriumet.
Til slutt produseres hormonet humant choriongonadotropin (HCG) i syncytiotrophoblast, som oppdages etter den andre uka av svangerskapet..
cytotrophoblast
For sin del danner cytotrofoblast det innerste laget av trofoblast. I utgangspunktet er det et uregelmessig lag av ovoide celler med en enkelt kjerne, og det er derfor de kalles mononukleære celler.
Cytotrofoblast er rett under syncytiotrofoblast og utviklingen begynner fra den første uka av svangerskapet. Trofoblastet letter embryoimplantasjonen gjennom cytotrofoblastceller, som har evne til å skille seg inn i forskjellige vev.
Den riktige utviklingen av cytotrofoblastceller er avgjørende for vellykket implantasjon av embryoet til livmor endometrium og er en svært regulert prosess. Imidlertid kan den ukontrollerte veksten av disse cellene generere tumorer, som for eksempel choriocarcinom..
utvikling
I løpet av den tredje uken inkluderer prosessen med embryonisk utvikling også den videre utviklingen av trofoblast. I utgangspunktet dannes de primære villi av den interne cytotrofoblast omgitt av det ytre lag av syncytiotrophoblast.
Deretter migrer cellene i den embryonale mesodermen mot den primære villuskjernen, og dette skjer i løpet av den tredje uken av svangerskapet. På slutten av denne uken begynner disse mesodermale cellene å singulere for å danne blodkarceller.
Som denne prosessen med celledifferensiering utvikler seg, vil det som er kjent som håret villøs system dannes. På dette punktet er placental villi dannet, som vil være den endelige.
Kapillærene som dannes fra denne prosessen vil senere komme i kontakt med andre kapillærer som dannes samtidig i mesodermen av korionplaten og fikseringsspedikken..
Disse nyopprettede karene kommer i kontakt med de i det intraembryoniske sirkulasjonssystemet. Således, i det øyeblikket hjertet begynner å slå (dette skjer i fjerde utviklingsuke) vil det villøse systemet være klar til å levere oksygen og næringsstoffer som er nødvendige for veksten.
Fortsatt med utviklingen, penetrerer cytotrofoblast enda mer i syncytiotrophoblasten som dekker håret, til de når morsendometometrium. De kommer i kontakt med noen hårete stilker og danner den eksterne cytotrofoblastiske dekket.
Dette laget går rundt trofoblasten og slutter å bli godt forbundet med kororplaten til endometrielt vev ved slutten av den tredje uken (dager 19-20) av svangerskapet..
Mens chorionisk hulrom har forstørret, er embryoen forankret til sin trofoblastiske dekning av fiksjonspedikken, en ganske smal bindestruktur. Deretter blir fikseringspedikken navlestrengen som forbinder placenta med embryoet.
referanser
- Cross, J.C. (1996). Trofoblast funksjon i normal og preeklamptisk graviditet. Foster- og modermedisinsk gjennomgang, 8(02), 57.
- Lunghi, L., Ferretti, M.E., Medici, S., Biondi, C., & Vesce, F. (2007). Kontroll av menneskelig trofoblastfunksjon. Reproduktiv Biologi og Endokrinologi, 5, 1-14.
- Pfeffer, P. L., & Pearton, D. J. (2012). Trofoblast utvikling. reproduksjon, 143(3), 231-246.
- Red Horse, K., Zhou, Y., Genbacev, O., Prakobphol, A., Foulk, R., McMaster, M., & Fisher, S.J. (2004). Trofoblast-differensiering under embryoimplantasjon og dannelse av maternale-fostergrensesnittet. Journal of Clinical Investigation, 114(6), 744-754.
- Screen, M., Dean, W., Cross, J.C., & Hemberger, M. (2008). Katepsinproteaser har forskjellige roller i trofoblastfunksjon og vaskulær remodeling. utvikling, 135(19), 3311-3320.
- Staun-Ram, E., & Shalev, E. (2005). Menneskelig trofoblastfunksjon under implantasjonsprosessen. Reproduktiv Biologi og Endokrinologi, 3(Figur 2), 1-12.
- Velicky, P., Knöfler, M., & Pollheimer, J. (2016). Funksjon og kontroll av humane invasive trofoblast subtyper: Intrinsic vs. mors kontroll. Celleadhesjon og migrasjon, 10(1-2), 154-162.


