Veier i pentosefaser og relaterte sykdommer
den sti av pentosen fosfat, også kjent som videremonoheksoser, er en fundamental metabolsk vei hvis sluttprodukt ribose nødvendig for synteseveier for nukleotider og nukleinsyrer, slik som DNA, RNA, ATP, NADH, FAD og koenzym A.
Det produserer også NADPH (nikotinamid-adenin-dinukleotidfosfat), brukt i forskjellige enzymatiske reaksjoner. Denne ruten er veldig dynamisk og i stand til å tilpasse sine produkter avhengig av cellens øyeblikkelige behov.
ATP (adenosintrifosfat) betraktes som "energimarginen" av cellen, fordi hydrolysen kan kobles til et bredt spekter av biokjemiske reaksjoner.
På lignende måte er en andre NADPH som kreves for reduktiv syntese av fettsyrer, kolesterol syntese, neurotransmitter syntese, fotosyntese og avgiftning reaksjoner energiverdi, inklusive.
Selv om NADPH og NADH er like i struktur, kan de ikke brukes om hverandre i biokjemiske reaksjoner. NADPH deltar i bruk av fri energi ved oksidasjon av visse metabolitter for reduktiv biosyntese.
I motsetning er NADH involvert i bruk av fri energi fra oksidasjon av metabolitter for å syntetisere ATP.
index
- 1 Historikk og plassering
- 2 funksjoner
- 3 faser
- 3.1 Oksidasjonsfase
- 3.2 Ikke-oksidativ fase
- 4 relaterte sykdommer
- 5 referanser
Historie og plassering
Indikasjonene på eksistensen av denne ruten begynte i år 1930 takket være etterforskeren Otto Warburg, til hvem oppdagelsen av NADP er tilskrevet ham+.
Enkelte observasjoner tillot oppdagelsen av ruten, spesielt fortsettelsen av respirasjon i nærvær av inhibitorer av glykolyse, slik som fluoridjonen.
Så, i 1950, fortalte forskerne Frank Dickens, Bernard Horecker, Fritz Lipmann og Efraim Racker pentosefosfatbanen.
Vevene som er involvert i syntese av kolesterol og fettsyrer, slik som brystkjertler, fettvev og nyrer, har høye konsentrasjoner av pentosfosfat-enzymer.
Leveren er også et viktig vev for denne vei: Omtrent 30% av oksydasjonen av glukose i dette vevet skjer takket være enzymer av pentosefosfatveien.
funksjoner
Pentosefosfatbanen er ansvarlig for å opprettholde hemostasen av karbon i cellen. På samme måte syntetiserer banen syntetiske forløpere av nukleotider og molekyler som er involvert i syntese av aminosyrer (strukturelle blokker av peptider og proteiner).
Det er den viktigste kilden til å redusere kraften for enzymatiske reaksjoner. I tillegg gir den de nødvendige molekylene for anabole reaksjoner og for forsvarsprosesser mot oksidativt stress. Den siste fasen av sporet er kritisk i redoks prosesser under stress situasjoner.
fasene
Den pentosefosfateveien svei består av to faser i cellens cytosol: oksydativ, NADPH-genererende oksydasjon av glukose-6-fosfat til ribose-5-fosfat; og en ikke-oksidativ, som innebærer interkonversjon av sukkene med tre, fire, fem, seks og syv karbonatomer.
Denne ruten presenterer delte reaksjoner med Calvins syklus og med Entner-Doudoroff-banen, som er et alternativ til glykolyse.
Oksidasjonsfase
Oksidative dehydrogenering fase starter med et molekyl glukose-6-fosfat på karbon 1. Denne reaksjonen katalyseres av enzymet glukose-6-fosfat dehydrogenase, som har en høy spesifisitet for NADP+.
Produktet av denne reaksjonen er 6-fosfonoglukono-5-lakton. Deretter hydrolyseres dette produktet av enzymet laktonase for å gi 6-fosfoglukonat. Sistnevnte forbindelse tas av enzymet 6-fosfoglukonatdehydrogenase og blir ribulose-5-fosfat.
Fosfopentosa isomerase-enzym katalyserer det siste trinnet i den oksyderende fasen, som involverer syntesen av ribose-5-fosfat ved isomerisering av ribulose-5-fosfat.
Denne reaksjonsserien produserer to molekyler NADPH og ett molekyl av ribose 5-fosfat per molekyl glukose 6-fosfat som kommer inn i denne enzymatiske vei.
I noen celler er NADPH-kravene større enn de for ribose-5-fosfat. Derfor tar transketolase og transaldolase enzymer ribose 5-fosfat og omdanner det til glyceraldehyd 3-fosfat og fruktose 6-fosfat, noe som gir vei til den ikke-oksidative fasen. Disse to siste forbindelsene kan komme inn i den glykolytiske banen.

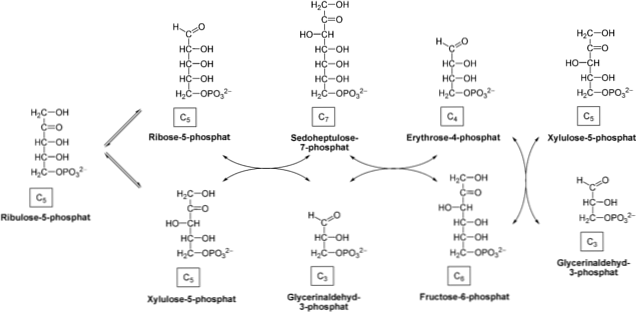
Ikke-oksidativ fase
Fasen begynner med en epimeriseringsreaksjon katalysert av enzymet pentose-5-fosfatepimerase. Ribulose-5-fosfat tas av dette enzymet og omdannes til xylulose-5-fosfat.
Produktet blir tatt opp av transketolase enzym som virker sammen med den koenzym tiaminpyrofosfat (TPP) som katalyserer passasje av xylulose-5-fosfat til ribose-5-fosfat. Ved overføring av ketose til aldose produseres glyceraldehyd-3-fosfat og sedoheptulose-7-fosfat.
Deretter transaldolase Enzymet overfører C3 molekylet sedoheptulose 7-fosfat til glyseraldehyd-3-fosfat, som frembringer en fire-karbonsukkeret (erytrose-4-fosfat) og en seks-karbon (fruktose-6 fosfat). Disse produktene er i stand til å mate den glykolytiske banen.
Enzymet virker transcetosala igjen for å overføre en C2-xylulose-5-fosfat til erytrose-4-fosfat, som fører til fruktose-6-fosfat og resultere glyseraldehyd-3-fosfat. Som i forrige trinn kan disse produktene gå inn i glykolyse.
Denne andre fasen forbinder veiene som genererer NADPH med de som er ansvarlige for å syntetisere ATP og NADH. I tillegg kan produktene fruktose-6-fosfat og glyceraldehyd-3-fosfat gå inn i glukoneogenesen.
Relaterte sykdommer
Ulike patologier er relatert til pentosefosfatets vei, mellom disse neuromuskulære sykdommene og ulike typer kreft.
De fleste kliniske studier fokuserer på å kvantifisere aktiviteten av glukose-6-fosfat dehydrogenase, fordi det er det viktigste enzymet som er ansvarlig for å regulere banen.
I blodlegemer som tilhører personer som er mottagelige for anemi, har de en lav enzymatisk aktivitet av glukose-6-fosfat dehydrogenase. I motsetning hevder cellelinjer relatert til karcinomer i strupehodet høy enzymaktivitet.
NADPH er involvert i produksjonen av glutation, et sentralt peptidmolekyl i beskyttelsen mot reaktive oksygenarter, involvert i oksidativ stress.
Ulike typer kreft fører til aktivering av pentoseveien og er forbundet med metastase, angiogenese og respons på kjemoterapi og strålebehandlinger.
På den annen side utvikler kronisk granulomatøs sykdom når det er mangel på produksjon av NADPH.
referanser
- Berg, J.M., Tymoczko, J. L., Stryer, L (2002). biokjemi. WH Freeman
- Konagaya, M., Konagaya, Y., Horikawa, H., & Iida, M. (1990). Pentosefosfatbane i nevromuskulære sykdommer-evaluering av muskelglukose 6-fosfat dehydrogenase aktivitet og RNA innhold. Rinsho shinkeigak. Klinisk nevrologi, 30(10), 1078-1083.
- Kowalik, M. A., Columbano, A., & Perra, A. (2017). Fremvoksende rolle av pentosefosfatveien i hepatocellulært karcinom. Grenser i onkologi, 7, 87.
- Patra, K. C., & Hay, N. (2014). Pentosefosfatveien og kreft. Trender i biokjemiske fag, 39(8), 347-354.
- Stincone, A., Prigione, A., Cramer, T., Wamelink, M., Campbell, K., Cheung, E., ... & Keller, M. A. (2015). Retur av metabolisme: biokjemi og fysiologi av pentosefosfatveien. Biologiske vurderinger, 90(3), 927-963.
- Voet, D., & Voet, J. G. (2013). biokjemi. Artmed Publisher.


