Smørsyreformel, egenskaper, risiko og bruk
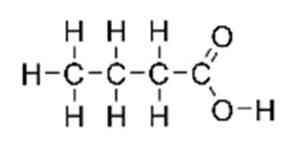
den smørsyre, også kjent som n-butansyre (i IUPAC-systemet), er det en karboksylsyre med strukturformelen CH3CH2CH2-COOH. Det er klassifisert som en kortkjedet fettsyre. Den har en ubehagelig lukt, skarp smak og samtidig litt søt (lik eter). Strukturen er illustrert i figur 1.
Det finnes spesielt i rancid smør, parmesanost, rå melk, animalsk fett, vegetabilske oljer og oppkast. Navnet er hentet fra det greske ordet βουτυρος, som betyr "smør" (bidragsytere, 2016).
Smørsyre dannes i humant kolon ved bakteriell gjæring av karbohydrater (inkludert kostfiber), og formentlig undertrykker kolorektal kreft.
Smørsyre er en fettsyre som forekommer i form av estere i animalsk fett og vegetabilske oljer. Interessant nok har estere med lav molekylvekt av smørsyre, så som metylbutyrat, hovedsakelig behagelige smaker eller smaker (det metabolomiske innovasjonssenteret, S.F.).
index
- 1 Fysiske og kjemiske egenskaper til smørsyre
- 2 Reaktivitet og farer
- 3 Bruker og fordeler for helse
- 4 referanser
Fysiske og kjemiske egenskaper til smørsyre
Smørsyre er en fargeløs væske med en ubehagelig lukt av rancid smør. Det har også en viss smak av smør.
Den har en molekylvekt på 88,11 g / mol og en densitet på 0,9528 g / ml ved romtemperatur. Smeltepunktet er -5,1 ° C og dets kokepunkt er 163,75 ° C.
Forbindelsen er oppløselig i vann, etanol og eter. Det er litt løselig i karbontetraklorid. Det er en svak syre, noe som betyr at den ikke dissocieres helt, dens pKa er 4,82 (National Center for Biotechnology Information, S.F.).
En isomer-2-metylpropansyre (isosmørsyre), (CH3) 2CHCO2H, er både fri tilstand og dens etylester i noen vegetabilske oljer. Selv om det er kommersielt mindre viktig enn smørsyre (Brown, 2011).
Smørsyre kan reagere med oksidasjonsmidler. Brennstoffreaksjoner forekommer med kromtrioksyd over 100 ° C. De er også uforenlige med baser og reduksjonsmidler. Kan angripe aluminium og andre lettmetaller (BUTYRIC ACID, 2016).
Reaktivitet og farer
Smørsyre anses som en brennbar forbindelse. Uforenelig med sterke oksidasjonsmidler, aluminium og de fleste andre vanlige metaller, alkalier, reduksjonsmidler (Royal Society of Chemistry, 2015).
Forbindelsen er meget farlig i tilfelle av kontakt med huden (som kan forårsake forbrenninger), ved svelging, ved øyenkontakt (irritament) og inhalering (kan forårsake alvorlig irritasjon av luftveiene).
Sprayvæske eller tåke kan forårsake vevskader, spesielt i slimhinner i øyne, munn og luftveier.
Stoffet er giftig for lungene, nervesystemet, slimhinner. Gjentatt eller langvarig eksponering for stoffet kan forårsake skade på disse organene, samt irritasjon av luftveiene som fører til hyppige angrep av bronkial infeksjon (Material Safety Data Sheet Butyric acid, 2013).
I tilfelle kontakt med øynene, bør det verifiseres hvis offeret har kontaktlinser og fjerner dem. Offrets øyne skal vaskes med vann eller vanlig saltvann i 20 til 30 minutter samtidig som du ringer til sykehus.
Ved kontakt med huden, skal det berørte området bli nedsenket i vann mens du fjerner og isolerer alle forurensede klær. Vask forsiktig alle berørte områder av huden med såpe og vann. Medisinsk oppmerksomhet må oppnås.
Ved innånding, bør du legge det forurensede området til et kjølig sted. Hvis symptomene utvikler seg (som hvæsen, hoste, kortpustethet eller brennende i munnen, halsen eller brystet), kontakt lege.
Ved inntak bør oppkast ikke fremkalles. Hvis offeret er bevisst og ikke har anfall, bør ett eller to glass vann administreres for å fortynne kjemikaliet og ringe til sykehus eller giftkontrollsentral.
Hvis offeret er kollapset eller ubevisst, ikke gi noe gjennom munnen, sørg for at offerets luftvei er åpen og plasser offeret på siden med hodet lavere enn kroppen. Umiddelbar medisinsk hjelp må oppnås.
Bruk og fordeler for helse
De lavmolekylære estere av smørsyre, så som metylbutyrat, har en lukt og smak, vanligvis hyggelig. På grunn av dette finner de bruk som mat og parfyme tilsetningsstoffer.
Butyrat, den konjugerte basen av smørsyre, finnes naturlig i flere matvarer. Det kan også legges som et supplement eller smaksstoff i andre.
Estere av smørsyre eller butyrater brukes til å lage kunstige smaker og essenser av vegetabilsk olje. Butylamyrat er en hovedbestanddel av aprikosolje, mens metylbutyrat finnes i ananasolje.
I tillegg blir brukt som et smaksgivende middel, er ananas oljen også brukes for å fremme benvekst, kurere tannlegekontor og behandle forkjølelse, sår hals og akutt sinusitis, i henhold til produsenten av naturlige produkter OCA Brasil (PULUGURTHA, 2015).
Bakterier funnet i mage-tarmkanalen kan produsere betydelige mengder fermenterende butyrat, kostfiber og ikke-fordøyelige karbohydrater. Å spise fiberrike matvarer som bygg, havre, brun ris og kli er en sunn måte å få butyrat i kroppen din.
En studie publisert i november 2010 utgaven av "Journal of Nutrition" indikerer at et måltid av korn om natten rik på ikke fordøyelige karbohydrater kunne øke konsentrasjonen av plasmabutyrat neste morgen.
Han legger til at dette kan være mekanismen som helkorn bidrar til å forebygge diabetes og hjertesykdom.
Smørsyre, som butyrat, er dannet i den humane kolon som et produkt av gjæring av fibrene, og det er foreslått som en faktor som forklarer hvorfor høy fiber dietter er beskyttende i forebygging av tykktarmskreft.
Vi har undersøkt flere hypoteser om den mulige mekanisme for dette forholdet, herunder om butyrat er viktig for å opprettholde normal fenotypisk ekspresjon av epitelceller, eller for å øke fjerning av skadede celler ved apoptose.
Andre fordeler med smørsyre eller butyrat er:
- Hjelp med vekttap.
- Lindrer irritert kolonsyndrom (Andrzej Załęski, 2013).
- Behandling av Crohns sykdom (Ax, S.F.).
- Bekjempe insulinresistens.
- Det har antiinflammatoriske effekter.
referanser
- Andrzej Załęski, A. B. (2013). Smørsyre i irritabel tarmsyndrom. Przegla̜d Gastroenterologiczny, 350-353. Hentet fra ncbi.nlm.nih.gov.
- Ax, J. (S.F.). Hva er smørsyre? 6 smørsyre fordeler du trenger å vite om. Hentet fra draxe: draxe.com.
- Brown, W. H. (2011, 2 desember). Smørsyre (CH3CH2CH2CO2H). Hentet fra encyklopedi britannica: Gjenopprettet fra britannica.com.
- BUTYRSYRE. (2016). Hentet fra cameokemikalier: cameochemicals.noaa.gov.
- bidragsytere, N. W. (2016, 22. desember). Smørsyre. Hentet fra New World Encyclopedia: Hentet fra newworldencyclopedia.org.
- Sikkerhetsdatablad Smørsyre. (2013, 21 mai). Hentet fra sciencelab: sciencelab.com.
- Nasjonalt senter for bioteknologisk informasjon. (S.F.). PubChem Compound Database; CID = 264. Hentet fra PubChem: ncbi.nlm.nih.gov.
- PULUGURTHA, S. (2015, 1. juni). Hvilke matvarer er høye i butyrat? Hentet fra livestrong: livestrong.com.
- Royal Society of Chemistry. (2015). Butansyre. Hentet fra chemspider: chemspider.com.
- det metabolomiske innovasjonssenteret. (S.F.). Human metabolome database viser metabocard for smørsyre. Hentet fra hmdb.no: hmdb.ca.


