Law of Boyle-Mariotte historie, matematisk uttrykk, eksempler
Loven til Boyle er det som uttrykker forholdet mellom trykket som utøves av eller på en gass og volumet okkupert av det; holder konstant temperaturen på gassen, så vel som dens mengde (antall mol).
Denne loven, sammen med Charles, Gay-Lussac, Charles og Avogadro, beskriver oppførelsen av en ideell gass; Spesielt i en lukket beholder gjenstand for volumendringer som utøves av en mekanisk kraft.
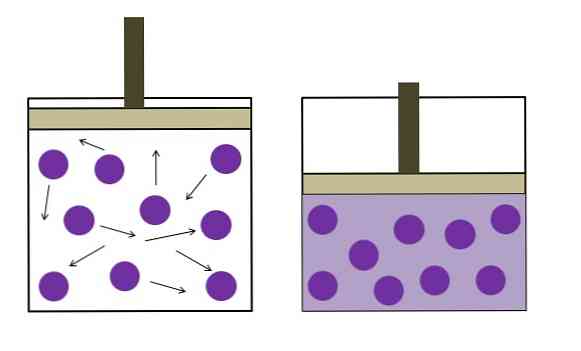
Bildet over oppsummerer kort Boyle-Mariotte-loven.
De lilla prikkene representerer molekyler eller gassatomer, som kolliderer med beholderens indre vegger (til venstre). Ved å redusere ledig plass eller volum av beholderen okkupert av denne gassen, øker kollisjonene, noe som betyr en økning i trykk (høyre).
Dette viser at trykket P og volum V av gassen er omvendt proporsjonale dersom beholderen er hermetisk forseglet; ellers ville et høyere trykk være lik en større utvidelse av beholderen.
Hvis en plot V ble laget mot P, med dataene for henholdsvis V og P på henholdsvis Y og X-aksene, ville en asymptotisk kurve bli observert. Jo mindre er V, jo større er økningen i P; det vil si at kurven vil strekke seg til høye verdier av P på X-aksen.
Selvfølgelig forblir temperaturen konstant; men hvis det samme eksperimentet ble utført ved forskjellige temperaturer, ville de relative posisjonene til disse kurvene V vs P endres i Cartesian-aksen. Forandringen ville være enda tydeligere hvis den ble plottet på en tredimensjonal akse, med konstant T på Z-aksen.
index
- 1 History of Boyle's law
- 1.1 Bakgrunn
- 1.2 Eksperiment med kvikksølv
- 1,3 Edme Mariotte
- 1.4 Styrking av loven
- 2 Hva består denne loven av??
- 3 Matematisk uttrykk
- 4 Hva er det for? Hvilke problemer løser Boyles lov??
- 4.1 Dampmaskiner
- 4.2 Sip drinker
- 4.3 Åndedrettsvern
- 5 Eksempler (eksperimenter)
- 5.1 Eksperiment 1
- 5.2 Eksperiment 2
- 6 Referanser
History of Boyle's law
bakgrunn
Siden forskeren Galileo Galilei uttrykte sin tro på tomhetens eksistens (1638), begynte forskere å studere egenskapene til luft og delvise hulrom.
Den engel-irske kjemikeren Robert Boyle begynte sin studie av luftegenskaper i 1638 da han lærte at Otto von Guericke, en tysk ingeniør og fysiker, hadde bygget en luftpumpe.
Eksperiment med kvikksølv
For å utføre sine studier av lufttrykk brukte Boyle et glassrør i form av "J", hvis konstruksjon ble tilskrevet Robert Hooke, en assistent av Boyle. Enden av den korte armen var forseglet, mens enden av rørets lange arm var åpen for å plassere kvikksølv.
Fra begynnelsen ønsket Boyle å studere luftens elastisitet, kvalitativt og kvantitativt. Ved å hente kvikksølv gjennom den åpne enden av det "J" formede røret utledde Boyle at luften i den korte armen av røret ble kontrahert under kvikksølvtrykk.
resultater
Jo større mengden kvikksølv er tilsatt til røret, jo større press utøves på luften og jo lavere er volumet. Boyle oppnådde en negativ eksponentiell type graf for luftvolum som en funksjon av trykk.
Selv om du plotter luftens volum mot omvendt trykk, har du en rett linje med positiv helling.
I 1662 publiserte Boyle den første fysiske loven som ble gitt i form av en ligning, som indikerte funksjonell avhengighet av to variabler. I dette tilfellet er trykket og volumet.
Boyle påpekte at det var et omvendt forhold mellom trykket som utøves på en gass og volumet okkupert av den gassen, og dette forholdet er relativt sant for ekte gasser. De fleste gasser oppfører seg som ideelle gasser ved moderat trykk og temperatur.
Med høyere trykk og lavere temperaturer ble avvik fra oppførselen til de virkelige gassene til idealer mer merkbare.
Edme Mariotte
Den franske fysikeren Edme Mariotte (1620-1684) oppdaget uavhengig av samme lov i 1679. Men det hadde fortjeneste å vise at volumet varierer med temperaturen. Det er derfor det heter Mariotte's Law eller Boyle og Mariotte's Law.
Styrking av loven
Daniel Bernoulli (1737) styrket Boyles lov ved å påpeke at trykk av en gass er produsert av virkningen av gasspartikler på veggene i beholderen som inneholder den..
I 1845 publiserte John Waterston en vitenskapelig artikkel, der han fokuserer på hovedprinsippene i kinetisk teori om gasser.
Senere konsoliderte Rudolf Clausius, James Maxwell og Ludqwig Boltzmann kinetisk teori om gasser, som relaterer trykket som utøves av en gass med hastigheten til partiklene av gassen i bevegelse.
Jo mindre volumet av beholderen som inneholder en gass, jo større er frekvensen av virkningen av partiklene som danner den mot veggene av beholderen; og derfor er jo større trykket utøves av gassen.
Hva består denne loven av??
Forsøkene utført av Boyle påpeker at det er et omvendt forhold mellom volumet okkupert av en gass og trykket som utøves på den. Imidlertid er ovennevnte forhold ikke helt lineært, som indikert ved en graf av volumvariasjon i henhold til trykket tilskrives Boyle.
I Boyle-loven er det påpekt at volumet opptatt av en gass er omvendt proporsjonalt med trykket. Det er også indikert at produktet av trykket av en gass ved sitt volum er konstant.
Matematisk uttrykk
For å komme til matematisk uttrykk for Boyle-Mariotte-loven, starter vi fra:
V α 1 / P
Hvor det indikerer at volumet opptatt av en gass er omvendt proporsjonalt med dets trykk. Imidlertid er det en konstant som dikterer hvordan omvendt proporsjonal dette forholdet er.
V = k / P
Hvor k er proportionalitetskonstanten. Clearing k du har:
VP = k
Produktet av trykket av en gass ved sitt volum er konstant. deretter:
V1P1 = k og v2P2 = k
Og fra dette kan det utledes at:
V1P1 = V2P2
Sistnevnte er det endelige uttrykket eller ligningen for Boyles lov.
Hva er det for? Hvilke problemer løser Boyles lov??
Dampmaskiner

Boyle-Mariotte lov gjelder for drift av dampmotorer. Det er en ekstern forbrenningsmotor som bruker transformasjonen av termisk energi fra en mengde vann til mekanisk energi.
Vannet oppvarmes i en hermetisk forseglet kjele, og den produserte dampen utøver et trykk i henhold til Boyle-Mariote-loven som gir en volumutvidelse av en sylinder ved å skyve et stempel.
Stempelets lineære bevegelse omformes til en rotasjonsbevegelse, ved bruk av et system med vev og vev, som kan kjøre hjulene til et lokomotiv eller rotoren til en elektrisk generator.
For tiden er den alternative dampmotor en liten brukt motor, siden den er blitt forskjøvet av den elektriske motoren og forbrenningsmotoren i transportkjøretøy.
Sipping drinker
Handlingen med å suge en brus eller juice fra en flaske gjennom et plastrør er knyttet til Boyle-Mariotte-loven. Når luften suges fra røret ved hjelp av munnen, er det en nedgang i trykket inne i røret.
Dette trykkfallet tilrettelegger oppoverbevegelsen av væsken i røret, slik at den inntakes. Det samme prinsippet fungerer i utvinning av blod ved hjelp av en sprøyte.
Åndedrettssystem
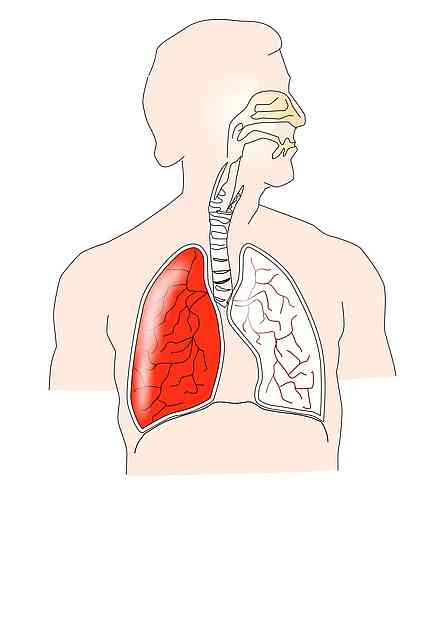
Boyle-Mariotte lov er nært knyttet til åndedrettssystemets funksjon. Under inspirasjonsfasen oppstår sammentrekning av membranen og andre muskler; for eksempel de eksterne intercostaler som produserer en utvidelse av ribbeholderen.
Dette medfører en reduksjon i intrapleuralt trykk, noe som forårsaker en lungekspansjon som gir en økning i lungevolumet. Derfor reduseres det intrapulmonale trykket i henhold til Boyle-Mariotte-loven.
Når det intrapulmonale trykket er subatmosfærisk, strømmer atmosfærisk luft inn i lungene, noe som resulterer i økt trykk i lungene; tilsvarer dens trykk på atmosfærisk trykk og avsluttende fase av inspirasjon.
Deretter slapper de inspirerende musklene av og de ekspiratoriske musklene trekker seg sammen. I tillegg opptrer lungelastisk tilbaketrekking, et fenomen som gir en nedgang i lungemengde, med en følgelig økning i intrapulmonaltrykk, noe som kan forklares av Boyle-Mariotte-loven..
Ved å øke intrapulmonaltrykket og bli større enn atmosfærisk trykk, flyter luften fra det indre av lungene inn i atmosfæren. Dette skjer til trykket utjevnes, som avslutter utløpsfasen.
Eksempler (eksperimenter)
Eksperiment 1
En liten ballong er plassert tett lukket, noe som gjør en knute i munnen, inne i en sprøyte, som stemplet er fjernet, på ca. 20 ml. Stemplet på sprøyten er plassert mot midtdelen av sprøyten, nålen er fjernet og luftinnløpet er blokkert.
observasjon
Ved langsomt å trekke stempelet på injeksjonsmidlet, observeres det at ballongen er oppblåst.
forklaring
To trykk utøves på ballongens veggen: et trykk på sitt indre ansikt, luftproduktet inne i ballongen og et annet trykk på ballongens ytre flate som utøves av luften inneholdt i sprøyten.
Når du trekker støpselet på injeksjonsinnretningen, opprettes et halvvakuum i det. Derfor reduseres lufttrykket på pumpeveggets ytre flate, noe som gjør trykket utøvet inne i pumpen relativt større..
Dette nettotrykket, i henhold til Boyle-Mariote-loven, vil produsere en spenning av ballongveggen og en økning i volumet av ballongen.
Eksperiment 2
Klipp en plastflaske, omtrent halvparten, og sørg for at kuttet er så horisontalt som mulig. I flasken er en veljustert ballong plassert, samtidig er en viss mengde vann plassert i en dyp parabolen.
observasjon
Ved å plassere bunnen av flasken med ballongen på vannet i parabolen, er ballongen moderat oppblåst.
forklaring
Vannet fortjener en viss mengde luft, noe som øker lufttrykket på flaskenes vegg og ballongens indre. Dette medfører, ifølge Boyle-Mariotte-loven, en økning i volumet av kloden, som er visualisert av verdens oppblåsning.
referanser
- Wikipedia. (2019). Boyle's lov. Hentet fra: en.wikipedia.org
- Editors of Encyclopaedia Britannica. (27. juli 2018). Boyle's lov. Encyclopædia Britannica. Hentet fra: britannica.com
- Helmenstine, Todd. (5. desember 2018). Formelen for Boyles lov. Hentet fra: thoughtco.com
- Unge indiske filmer. (15. mai 2018). Boyle's Law: Science Experiment For Kids. Hentet fra: yifindia.com
- Cecilia Bembibre (22. mai 2011). Varmluftsballong Definisjon ABC. Hentet fra: definicionabc.com
- Ganong, W, F. (2003). Medisinsk fysiologi (19. utgave). Redaksjonell den moderne håndboken.


