Etylacetatstruktur, egenskaper, syntese, bruk og risiko
den etylacetat eller etyletanoat (IUPAC navn) er en organisk forbindelse hvis kjemiske formel er CH3COOC2H5. Den består av en ester, hvor alkoholkomponenten stammer fra etanol, mens karboksylsyrekomponenten kommer fra eddiksyre.
Det er en væske under normale forhold med temperatur og trykk, og gir en behagelig aroma til frukt. Denne egenskapen kommer helt i harmoni med det som forventes av en ester; som faktisk er den kjemiske naturen av etylacetat. Av denne grunn finner den bruk i matvarer og alkoholholdige drikker.
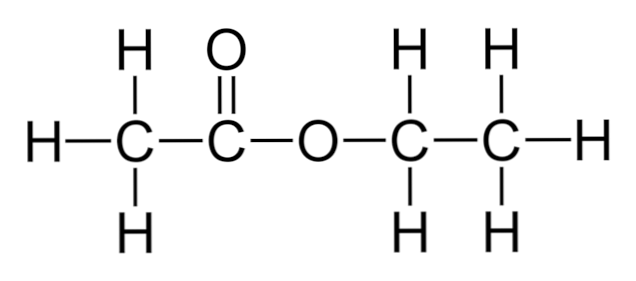
I det øvre bildet er strukturskjelettet av etylacetat vist. Merk til venstre sin karboksylsyrekomponent, og til høyre alkoholkomponenten. Fra et strukturelt synspunkt kan det forventes at denne forbindelsen oppfører seg som en hybrid mellom eddik og alkohol; Det viser imidlertid egenskaper.
Dette er hvor slike hybrider kalt estere skiller seg ut som å være forskjellige. Etylacetat kan ikke reagere som en syre, og det kan heller ikke dehydrere i fravær av en OH-gruppe. I stedet gjennomgår det grunnleggende hydrolyse i nærvær av en sterk base, så som natriumhydroksyd, NaOH.
Denne hydrolysereaksjonen brukes i undervisningslaboratorier for kjemiske kinetiske eksperimenter; hvor reaksjonen i tillegg er av andre rekkefølge. Når hydrolyse oppstår, returnerer praktisk talt etyletanoat til sine opprinnelige komponenter: syre (deprotonert av NaOH) og alkohol.
I sitt strukturelle skjelett blir det observert at hydrogenatomer dominerer over oksygen. Dette påvirker deres evne til å samhandle med ikke-polare arter som fett. Det brukes også til å oppløse forbindelser som harpiks, fargestoffer og generelt organiske faste stoffer.
Til tross for å ha en behagelig aroma, gir en langvarig eksponering for denne væsken en negativ innvirkning (som nesten alle kjemiske forbindelser) i kroppen.
index
- 1 Struktur av etylacetat
- 1.1 Fravær av hydrogendonoratomer
- 2 Fysiske og kjemiske egenskaper
- 2.1 navn
- 2.2 Molekylær formel
- 2,3 Molekylvekt
- 2.4 Fysisk beskrivelse
- 2,5 farge
- 2,6 lukt
- 2,7 Smak
- 2,8 Luktgrense
- 2,9 kokepunkt
- 2,10 Smeltepunkt
- 2.11 Løselighet i vann
- 2.12 Løselighet i organiske løsningsmidler
- 2.13 tetthet
- 2.14 Damptetthet
- 2,15 Stabilitet
- 2.16 Damptrykk
- 2,17 Viskositet
- 2.18 Forbrenningsvarme
- 2.19 Fordampingsvarme
- 2.20 Overflatespenning
- 2.21 Brekningsindeks
- 2.22 Lagertemperatur
- 2,23 pKa
- 3 Sammendrag
- 3.1 Fishers reaksjon
- 3.2 Tishchenko reaksjon
- 3.3 Andre metoder
- 4 bruksområder
- 4.1 Løsemiddel
- 4.2 Kunstige smaker
- 4.3 Analytics
- 4.4 Organisk syntese
- 4,5 kromatografi
- 4.6 Entomologi
- 5 risikoer
- 6 Referanser
Struktur av etylacetat
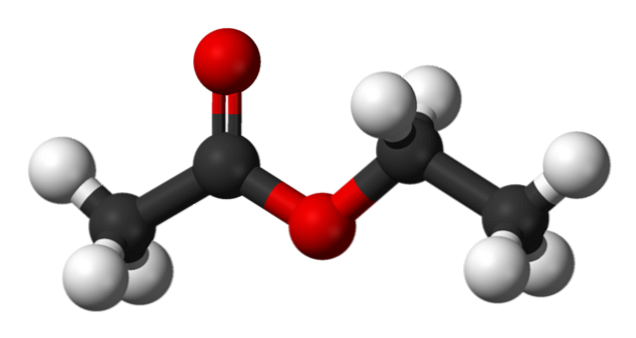
I det øvre bildet er strukturen av etylacetat vist med en modell av kuler og barer. I denne modellen er oksygenatomer med røde kuler uthevet; til venstre er fraksjonen avledet fra syren, og til høyre er fraksjonen avledet fra alkohol (alkoksygruppe, -OR).
Karbonylgruppen er verdsatt av C = O-bindingen (de dobbelte stenger). Strukturen rundt denne gruppen og det tilstøtende oksygen er flatt, fordi det er en delokalisering av lasten ved resonans mellom begge oksygenene; faktum som forklarer en relativt lav surhet av a-hydrogenene (de av -CH-gruppen3, knyttet til C = O).
Molekylet, ved å rotere to av sine bindinger, favoriserer direkte hvordan det interagerer med andre molekyler. Tilstedeværelsen av de to oksygenatomene og asymmetrien i strukturen gir den et permanent dipolmoment; som igjen er ansvarlig for deres dipol-dipol-interaksjoner.
For eksempel er den elektroniske tettheten større i nærheten av de to oksygenatomene, noe som avtar betydelig i gruppen -CH3, og gradvis i OCH-gruppen2CH3.
På grunn av disse interaksjonene danner etylacetatmolekylene en væske under normale forhold, som har et betydelig høyt kokepunkt (77ºC).
Fravær av donoratomer av hydrogenbindinger
Hvis du ser nøye på strukturen, vil du legge merke til fraværet av et atom som er i stand til å donere en hydrogenbro. Imidlertid er oksygenatomer slike akseptorer, og etylacetat er meget løselig i vann og samhandler i betydelig grad med polære forbindelser og hydrogenbindingsdonorer (slik som sukkerarter).
Også, dette lar deg samhandle godt med etanol; Derfor er dets tilstedeværelse i alkoholholdige drikkevarer ikke overraskende.
På den annen side gjør sin alkoksygruppe det i stand til å interagere med visse apolære forbindelser, så som kloroform, CH3cl.
Fysiske og kjemiske egenskaper
navnene
-Etylacetat
-Etyletanoat
-Eddiksyreester
-Acetoxietano
Molekylær formel
C4H8O2 eller CH3COOC2H5
Molekylvekt
88 106 g / mol.
Fysisk beskrivelse
Klar fargeløs væske.
farge
Fargeløs væske.
lukt
Karakteristisk for etere, ligner lukten av ananas.
smaken
Hyggelig når fortynnet, legger til en fruktig smak til øl.
Luktgrense
3,9 ppm. 0,0196 mg / m3 (lav lukt); 665 mg / m3 (høy lukt).
Detekterbar lukt ved 7 - 50 ppm (middel = 8 ppm).
Kokepunkt
171 ° F til 760 mmHg (77,1 ° C).
Smeltepunkt
-118,5 ºF (-83,8 ºC).
Løselighet i vann
80 g / l.
Løselighet i organiske løsningsmidler
Blandbar med etanol og etyleter. Meget løselig i aceton og benzen. Blandbar også med kloroform, faste og flyktige oljer, og også med oksygen- og klorerte løsningsmidler.
tetthet
0,9003 g / cm3.
Damptetthet
3,04 (i luftforhold: 1).
stabilitet
Den dekomponerer sakte med fuktighet; inkompatibel med flere plast og sterke oksidasjonsmidler. Blandingen med vann kan være eksplosiv.
Damptrykk
93,2 mmHg ved 25 ºC
viskositet
0,423 mPoise ved 25 ºC.
Forbrenningsvarme
2 238,1 kJ / mol.
Fordampingsvarme
35,60 kJ / mol ved 25 ºC.
Overflatespenning
24 dyn / cm ved 20 ºC.
Brytningsindeks
1,373 ved 20 ºC / D.
Lagringstemperatur
2 - 8 ºC.
pKa
16 - 18 ved 25 ºC.
syntese
Fisher reaksjon
Etylacetat syntetiseres industrielt ved Fisher-reaksjonen, hvor etanol blir forestret med eddiksyre. Reaksjonen utføres ved romtemperatur.
CH3CH2OH + CH3COOH <=> CH3COOCH'er2CH3 + H2O
Reaksjonen akselereres ved syrekatalyse. Likevekten beveger seg til høyre, det vil si mot produksjon av etylacetat, gjennom fjerning av vann; i henhold til loven om massehandling.
Reaksjon av Tishchenko
Etylacetat fremstilles også industrielt ved bruk av Tishchenko-reaksjonen, konjugering av to ekvivalenter av acetaldehyd ved bruk av et alkoksid som katalysator.
2 CH3CHO => CH3COOCH'er2CH3
Andre metoder
-Etylacetat syntetiseres som et koprodukt i oksydasjonen av butan til eddiksyre i en reaksjon utført ved en temperatur på 175 ° C og 50 atm-trykk. Kobolt og kromioner brukes som katalysator.
-Etylacetat er et koprodukt av etanolysen av polyvinylacetat til polyvinylalkohol.
-Etylacetat fremstilles også i industrien ved dehydrogenering av etanol, idet reaksjonen blir katalysert ved bruk av kobber ved forhøyet temperatur, men lavere enn 250 ° C..
søknader
Oppløsningsmidlet
Etylacetat brukes som løsningsmiddel og fortynningsmiddel som brukes ved rengjøring av kretskort. Den brukes som løsningsmiddel ved fremstilling av det modifiserte humleekstraktet og i koffeinering av kaffe og teblader. Den brukes i blekkene som brukes til å markere frukt og grønnsaker.
Etylacetat brukes i tekstilindustrien som et rengjøringsmiddel. Det brukes i kalibrering av termometre, brukt i separering av sukker. I malingsindustrien brukes den som løsemiddel og fortynningsmiddel av materialene som brukes.
Kunstige smaker
Den brukes i utarbeidelsen av frukt smaker; For eksempel: banan, pære, fersken og ananas, samt drue aroma, etc..
analytisk
Det brukes til bestemmelse av vismut, bor, gull, molybden og platina, samt thallium løsningsmiddel. Etylacetat har evnen til å ekstrahere mange forbindelser og elementer som er tilstede i vandig løsning, for eksempel: fosfor, kobolt, wolfram og arsen.
Organiske synteser
Etylacetat brukes i industrien som viskositetsreduksjonsmiddel for harpikser anvendt i fotoresistformuleringer. Det brukes til produksjon av acetamid, acetylacetat og metylheptanon.
kromatografi
I laboratoriene benyttes etylacetat som mobil fase av kolonnekromatografi og som ekstraksjonsløsningsmiddel. Ved å ha etylacetatet et relativt lavt kokepunkt, er det lett å fordampe, noe som gjør det mulig å konsentrere de oppløste substansene i løsningsmidlet.
entomologi
Etylacetat brukes i entomologi til asfykserende insekter plassert i en beholder, noe som gjør det mulig å samle og studere. Dampene i etylacetat dræper insektet uten å ødelegge det og forhindre dets herding, noe som gjør det lettere å samle seg sammen.
risikoer
-LD50 av etylacetat hos rotter indikerer lav giftighet. Det kan imidlertid irritere huden, øynene, huden, nesen og halsen.
-Eksponering for høye nivåer kan forårsake svimmelhet og svimmelhet. Også, langsiktig eksponering kan påvirke lever og nyre.
-Innånding av etylacetat i en konsentrasjon på 20.000 - 43.000 ppm kan forårsake lungeødem og blødning.
-Den yrkesmessige eksponeringsgrensen er satt av OSHA ved 400 ppm i luften, i gjennomsnitt, under et 8-timers arbeidsskifte.
referanser
- Steven A. Hardinger. (2017). Illustrert ordliste for organisk kjemi: etylacetat (EtOAc). Hentet fra: chem.ucla.edu
- Graham Solomons T.W., Craig B. Fryhle. (2011). Organisk kjemi. Aminer. (10th utgaven.). Wiley Plus.
- Morrison, R. T. og Boyd, R. N. (1990). Organisk kjemi (5tA utgave). Redaktør Addison-Wesley Iberoamericana.
- Wikipedia. (2019). Etylacetat. Hentet fra: en.wikipedia.org
- Bomull S. (s.f.). Etylacetat. Hentet fra: chm.bris.ac.uk
- Pubchem. (2019). Etylacetat. Hentet fra: pubchem.ncbi.nlm.nih.gov
- Newseed Chemical. (2018). Anvendelser og anvendelser av etylacetat. Hentet fra: foodweeteners.com
- New Jersey Department of Health of Senior Services. (2002). Etylacetat. [PDF]. Hentet fra: nj.gov


