Hydrobromsyre (HBr) struktur, egenskaper, formasjon, bruk
den Hydrobromsyre er en uorganisk forbindelse som resulterer fra den vandige oppløsningen av en gass som kalles hydrogenbromid. Dens kjemiske formel er HBr, og kan betraktes på forskjellige måter, tilsvarende: som et molekylhydrid eller et hydrogenhalogenid i vann; det vil si et hydrazid.
I kjemiske ligninger skal det skrives som HBr (ac), for å indikere at det er brombrint og ikke gass. Denne syren er en av de sterkeste kjente, enda mer enn saltsyre, HCl. Forklaringen på dette ligger i naturen av dets kovalente binding.
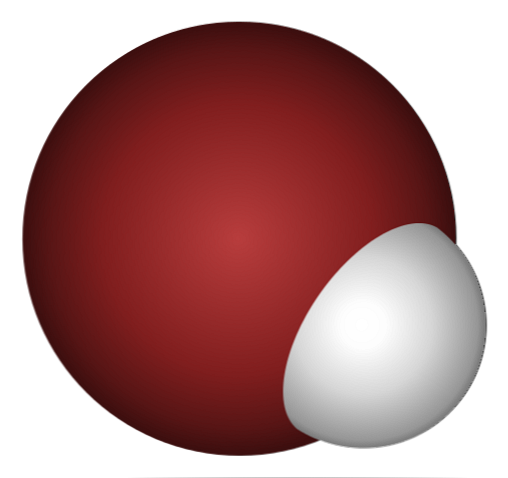
Hvorfor er HBr en slik syre, og enda mer oppløst i vann? Fordi det kovalente bindingen H-Br er svært svakt, på grunn av den dårlige overlapping av 1s-orbitalene av H og 4p av Br.
Dette er ikke overraskende hvis du ser nøye på bildet ovenfor, hvor klart bromatomet (brunt) er mye større enn hydrogenatomet (hvitt).
Følgelig forårsaker forstyrrelser nedbrytningen av H-Br-bindingen, frigjøring av H-ionet+. Deretter er hydrobromsyren en Brönsted-syre, siden den overfører protoner eller hydrogenioner. Dens styrke er slik at den brukes i syntesen av flere organobromerte forbindelser (som 1-brometan, CH3CH2Br).
Hydrobromsyre er, etter hydrisk, HI, en av de sterkeste og mest nyttige hydroksyder for fordøyelsen av visse faste prøver.
index
- 1 Struktur av hydrobromsyre
- 1.1 surhet
- 2 Fysiske og kjemiske egenskaper
- 2.1 Molekylær formel
- 2,2 Molekylvekt
- 2.3 Fysisk utseende
- 2.4 lukt
- 2,5 Luktgrense
- 2,6 tetthet
- 2,7 Smeltepunkt
- 2,8 kokepunkt
- 2.9 Løselighet i vann
- 2.10 Damptetthet
- 2,11 pKa surhet
- 2.12 Kalorikapasitet
- 2.13 Standard molarenthalpi
- 2.14 Standard molar entropi
- 2.15 Flammepunkt
- 3 Nomenklatur
- 4 Hvordan er det dannet?
- 4.1 Blanding av hydrogen og brom i vann
- 4.2 Fosfortribromid
- 4.3 Svoveldioksid og brom
- 5 bruksområder
- 5.1 Fremstilling av bromider
- 5.2 Syntese av alkylhalogenider
- 5.3 katalysator
- 6 Referanser
Struktur av hydrobromsyre
Strukturen til H-Br er vist på bildet, hvis egenskaper og karakteristika, selv de av gassen, er nært relatert til dets vandige løsninger. Derfor kommer det et punkt der du kommer i forvirring om hvilken av de to forbindelsene som er referert til: HBr eller HBr (ac).
Strukturen til HBr (ac) er forskjellig fra HBr, fordi vannmolekyler nå solvatiserer dette diatomiske molekylet. Når den er nær nok, overføres H+ til et H-molekyl2Eller som angitt i den følgende kjemiske ligningen:
HBr + H2O => Br-- + H3O+
Således består strukturen av hydrobromsyren av Brioner-- og H3O+ interaksjon elektrostatisk. Nå er det litt annerledes enn det kovalente bindingen til H-Br.
Dens store surhet skyldes den store anionen Br- kan knapt samhandle med H3O+, kan ikke forhindre ham i å overføre H+ til en annen omgivende kjemisk art.
surt
For eksempel er Cl- og F- selv om de ikke danner kovalente bindinger med H3O+, de kan interagere gjennom andre intermolekylære krefter, som hydrogenbroer (som bare F- er i stand til å akseptere dem). Hydrogenbroene F--H-OH2+ "Hinder" donasjonen av H+.
Det er av denne grunn at flussyre, HF, er en svakere syre i vann enn hydrobromsyre; siden de ioniske interaksjonene Br- H3O+ ikke bry deg om overføringen av H+.
Selv om vann er til stede i HBr (ac), er dens oppførsel ved slutten av kontoen lik den for et H-Br-molekyl; det er en H+ Det overføres fra HBr eller Br-H3O+.
Fysiske og kjemiske egenskaper
Molekylær formel
HBr.
Molekylvekt
80.972 g / mol. Merk at, som nevnt i forrige avsnitt, anses bare HBr og ikke vannmolekylet. Hvis molekylvekten er tatt fra formelen Br-H3O+ det ville ha en verdi på 99 g / mol omtrent.
Fysisk utseende
Fargeløs eller blekgul væske, som avhenger av konsentrasjonen av oppløst HBr. Jo mer gul det er, desto mer konsentrert og farlig vil det være.
lukt
Acrid, irriterende.
Luktgrense
6,67 mg / m3.
tetthet
1,49 g / cm3 (vandig løsning ved 48% vekt / vekt). Denne verdien, som de som svarer til smeltepunktet og kokpunktene, avhenger av mengden HBr oppløst i vannet.
Smeltepunkt
-11ºC (12ºF, 393ºK) (vandig løsning ved 49% vekt / vekt).
Kokepunkt
122 ° C (252 ° F 393 ° K) ved 700 mmHg (vandig løsning 47-49% vekt / vekt).
Løselighet i vann
-221 g / 100 ml (ved 0 ºC).
-204 g / 100 ml (15 ºC).
-130 g / 100 ml (100 ºC).
Disse verdiene refererer til gassformig HBr, ikke til hydrobromsyre. Som det kan sees, øker temperaturen oppløseligheten av HBr; oppførsel som er naturlig i gasser. Derfor, hvis konsentrerte HBr (ac) løsninger er påkrevd, er det bedre å jobbe med dem ved lave temperaturer.
Ved arbeid ved høye temperaturer vil HBr unnslippe i form av gassformige diatomære molekyler, så reaktoren må være forseglet for å hindre lekkasje.
Damptetthet
2,71 (i forhold til luft = 1).
Surhet pKa
-9.0. Denne konstante så negative er indikativ for sin store styrke av surhet.
Calorisk kapasitet
29,1 kJ / mol.
Standard molarenthalpi
198,7 kJ / mol (298 ºK).
Standard molar entropi
-36,3 kJ / mol.
Tennspunkt
Ikke brannfarlig.
nomenklatur
Navnet "hydrobromsyre" kombinerer to fakta: forekomsten av vann, og at brom har en valens på -1 i forbindelsen. På engelsk er det noe mer tydelig: hydrobromsyre, der prefikset "hydro" (eller hydro) refererer til vann; selv om det egentlig også kan referere til hydrogen.
Brom har en valens på -1 fordi den er bundet til hydrogenatom mindre elektronegativ enn den er; men hvis det er knyttet eller interaksjon med oksygenatomer, kan det ha mange valenser, for eksempel: +2, +3, +5 og +7. Med H kan bare adoptere en enkelt valens, og det er derfor suffikset -ico legges til navnet.
Mens HBr (g), hydrogenbromid, er vannfritt; det vil si, det har ikke vann. Derfor er det oppkalt under andre nomenklaturstandarder, tilsvarende det for hydrogenhalogenider.
Hvordan er det dannet?
Det finnes flere syntetiske metoder for å forberede hydrobromsyre. Noen av dem er:
Blanding av hydrogen og brom i vann
Uten å beskrive de tekniske detaljer, kan denne syre oppnås fra den direkte blanding av hydrogen og brom i en reaktor fylt med vann.
H2 + Br2 => HBr
På denne måten, som HBr danner, oppløses det i vannet; Dette kan trekke det i destillasjonene, slik at løsninger kan trekkes ut med forskjellige konsentrasjoner. Hydrogen er en gass, og brom er en mørk rødlig væske.
Fosfortribromid
I en mer utførlig prosess blandes sand, hydratisert rødt fosfor og brom. Vannfeller er plassert i isbader for å hindre at HBr rømmer og danner i stedet hydrobromsyre. Reaksjonene er:
2P + 3Br2 => 2PBr3
PBr3 + 3 H2O => 3HBr + H3PO3
Svoveldioksid og brom
En annen måte å forberede er på å reagere brom med svoveldioksid i vann:
Br2 + SW2 + 2H2O => 2HBr + H2SW4
Dette er en redoksreaksjon. The Br2 det reduserer, det tjener elektroner, ved å knytte sammen med hydrogenene; mens sjefen2 det oksiderer, det mister elektroner når det danner mer kovalente bindinger med andre oksygen, som i svovelsyre.
søknader
Fremstilling av bromider
Bromsaltene kan fremstilles dersom HBr (ac) blir omsatt med et metallhydroksyd. For eksempel vurderes produksjonen av kalsiumbromid:
Ca (OH)2 + 2HBr => CaBr2 + H2O
Et annet eksempel er for natriumbromid:
NaOH + HBr => NaBr + H2O
Således kan mange av de uorganiske bromider fremstilles.
Syntese av alkylhalogenider
Og hva med organiske bromider? Disse er organobrominerte forbindelser: RBr eller ArBr.
Dehydrering av alkoholer
Råmaterialet for å skaffe dem kan være alkoholer. Når de er protonert av surheten til HBr, danner de vann, som er en god utgående gruppe, og i stedet er det voluminøse atomet av Br innarbeidet, som vil bli kovalent bundet til karbonet:
ROH + HBr => RBr + H2O
Denne dehydrering utføres ved temperaturer over 100 ° C for å lette bruken av R-OH-bindingen2+.
Tilsetning til alkener og alkyner
HBr-molekylet kan tilsettes fra sin vandige løsning til dobbelt- eller trippelbindingen av en alken eller alkyn:
R2C = CR2 + HBr => RHC-CRBr
RC = CR + HBr => RHC = CRBr
Flere produkter kan oppnås, men under enkle forhold blir produktet først dannet der brom er koblet til et sekundært, tertiært eller kvaternært karbon (Markovnikov-regelen).
Disse halogenider griper inn i syntesen av andre organiske forbindelser, og deres anvendelsesområde er meget omfattende. Også noen av dem kan til og med brukes til syntese eller design av nye stoffer.
Ethereal clivage
Fra eterene kan to alkylhalogenider oppnås samtidig, idet hver bærer en av de to sidekjeder R eller R 'i den første eter R-O-R'. Det skjer noe som ligner på dehydrering av alkoholer, men reaksjonsmekanismen er forskjellig.
Reaksjonen kan skjematiseres med den følgende kjemiske ligning:
ROR '+ 2HBr => RBr + R'Br
Og vann er også utgitt.
katalysatoren
Syrligheten er slik at den kan brukes som en effektiv syrekatalysator. I stedet for å legge til Br anion- til molekylær struktur, åpner veien for et annet molekyl for å gjøre det.
referanser
- Graham Solomons T.W., Craig B. Fryhle. (2011). Organisk kjemi. Aminer. (10th utgaven.). Wiley Plus.
- Carey F. (2008). Organisk kjemi (Sjette utgave). Mc Graw Hill.
- Steven A. Hardinger. (2017). Illustrert ordliste for organisk kjemi: Hydrobromsyre. Hentet fra: chem.ucla.edu
- Wikipedia. (2018). Hydrobromsyre. Hentet fra: en.wikipedia.org
- Pubchem. (2018). Hydrobromsyre. Hentet fra: pubchem.ncbi.nlm.nih.gov
- Nasjonalt institutt for sikkerhet og hygiene på arbeidsplassen. (2011). Hydrogenbromid [PDF]. Hentet fra: insht.es
- PrepChem. (2016). Fremstilling av hydrobromsyre. Hentet fra: prepchem.com


