Propylen Kjemisk struktur, egenskaper og bruksområder
den propylen eller propen ved romtemperatur og ved atmosfærisk trykk er i gassform og, som andre alkener, er fargeløs. Det har en lukt som ligner på olje, men med mindre intensitet. Det har et dipol-øyeblikk siden, selv om det mangler en sterk polar kobling, er molekylet asymmetrisk.
Propylen er også en strukturell isomer av cyklopropan (de har samme kjemiske formel C)3H6). Det forekommer i naturen som følge av vegetasjon og gjæringsprosesser. Kunstig forekommer under behandling av fossile brensler som olje, naturgass og, i mindre grad, karbon.

På samme måte er etylen og propylen produkter av petroleumraffinering i en prosess for å splitte store hydrokarbonmolekyler for å generere små hydrokarboner med høy etterspørsel..
Propylen kan også oppnås ved å bruke forskjellige metoder:
- Reagerer reversibel etylen og buten, hvor de doble bindingene brytes og omformeres for å gi propylen.
- Gjennom en prosess av dehydrogenering (hydrogen tap) av propan.
- Som en del av et program for produksjon av olefiner fra metanol (MTO) ble propylen produsert fra metanol. Dette ble ført gjennom zeolittkatalysatoren, som fremmer dens dehydrering og fører til dannelsen av etylen og propylen.
3CH3OH (metanol) => CH3CH = CH2 (propylen) + 3H2O (vann)
index
- 1 Kjemisk struktur
- 2 Egenskaper
- 2,1 Molekylvekt
- 2.2 kokepunkt
- 2.3 Smeltepunkt
- 2.4 Flammepunkt
- 2,5 Løselighet
- 2.6 Løselighet uttrykt som masse
- 2,7 tetthet
- 2,8 Damptetthet
- 2.9 Damptrykk
- 2.10 Selvantennelse
- 2.11 Viskositet
- 2.12 Forbrenningsvarme
- 2.13 Fordampingsvarme
- 2.14 Overflatespenning
- 2.15 Polymerisering
- 2.16 Frysepunkt
- 2.17 Luktgrense
- 3 bruksområder
- 3.1 Polypropylen
- 3,2 akrylonitril
- 3.3 Propylenoksid
- 3.4 For syntese av alkoholer og andre anvendelser
- 4 referanser
Kjemisk struktur
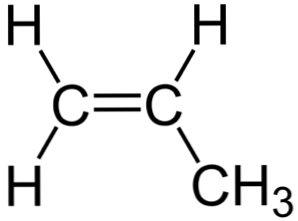
På bildet over kan man se den kjemiske strukturen av propylen, hvor asymmetrien skiller seg ut (høyre side er forskjellig fra venstre). Dens karbonskjelett, ikke inkludert H-atomer, kan observeres som en boomerang.
Denne boomerang presenterer en umettethet eller dobbeltbinding på en av dens sider (C1), og derfor er den flat på grunn av sp hybridisering2 av karbonatomer.
Imidlertid er den andre siden okkupert av metylgruppen (-CH3), hvis hybridisering er sp3 og den har en tetrahedral geometri. Således sett fra forsiden, er boomeranget flatt med H-atomer som stikker ut fra dette ved 109,5º omtrentlig.
I gassfasen påvirker molekylet svakt med andre ved dispersjonskrefter. Også forhindres interaksjonene mellom dobbeltbindingene (π-π) av to propylenmolekyler av metylgruppen.
Dette resulterer i en reduksjon av deres intermolekylære krefter, som reflekteres i deres fysiske egenskaper. Bare ved svært lave temperaturer kan propylen vedta en solid struktur, der boomeran forblir gruppert med sine svake vekselvirkninger.
egenskaper
Det er en fargeløs gass med en aromatisk lukt. Den transporteres som flytende gass, og, når det slipper ut av karene som inneholder den, som gjør gass eller væske. Ved lave konsentrasjoner danner det en eksplosiv og brennbar blanding med luft, idet tettheten av propylen er høyere enn luften.
Molekylvekt
42,081 g / mol
Kokepunkt
53,9 ºF til 760 mmHg
48 ºC til 760 mmHg
Smeltepunkt
301.4 ºF
185 ºC
Flammepunkt
162 ºF
løselighet
44,6 ml / 100 ml i vann.
1.250 ml / 100 ml i etanol.
524,5 ml / 100 ml i eddiksyre.
Løselighet uttrykt som masse
200 mg / l 25 ºC
tetthet
0,609 mg / ml ved -52,6º F
0,5139 ved 20 ° C
Damptetthet
1,46 til 32 ° F (i forhold til luft tatt som referanse).
1,49 (luft = 1).
1,91 kg / m3 til 273,15 ºK
Damptrykk
1 mmHg ved -205.4ºF
760 mmHg til -53,9 ° F
8,69 × 103 mmHg ved 25 ºC (ekstrapolert verdi).
1,158 kPa ved 25 ºC
15,4 atm ved 37 ºC
selvantennelse
851 ºF
455 ºC
viskositet
83,4 mikropoise ved 16,7 ºC.
Forbrenningsvarme
16.692 BTU / lb
10.940 cal / g
Fordampingsvarme
104,62 cal / g (ved kokepunktet)
Overflatespenning
16,7 dyn / cm ved 90 ° C
polymerisasjon
Polymeriserer ved høye temperaturer og høye trykk i nærvær av katalysatorer.
Frysepunkt
185,25 ° C.
Luktgrense
10-50 mg / m3 (Detection)
100 mg / m3 (Recognition)
søknader

Den brukes i petrokjemisk industri som drivstoff og alkyleringsmiddel. I kjemisk industri brukes den som råmateriale til produksjon og syntese av mange derivater.
Den har hovedsakelig bruk av polypropylen, akrylnitril (ACN), propylenoksyd (PO), alkoholer, kumen- og akrylsyrer.
polypropylen
Polypropylen er en av de viktigste plastmaterialene som brukes i elektronikk og elektrisk tilbehør, husholdningsartikler, flaskehatter og kofferter.
Det laminerte materialet brukes i emballasje av søtsaker, etiketter, CDer, etc., mens fibre er laget av mapper og klær..
akrylnitril
Elastomere polymerer og fibre er oppnådd fra akrylonitril. Disse fibrene er ment for produksjon av forskjellige former for klær, for eksempel gensere, sokker og sportsklær. De brukes også i hjemmemøbler, i mapper, polstring, puter og tepper.
Propylenoksyd
Propylenoksyd deltar som en komponent i syntesen av polyuretan. Dette brukes til fremstilling av fleksibelt skum og stivt skum. Fleksibelt skum brukes som fyllstoff til hjemmemøbler og i bilindustrien.
På den annen side er stivt skum hovedsakelig brukt som byggisolasjonsmateriale.
I tillegg benyttes propylenoksid til fremstilling av propylenglykol. Denne forbindelsen brukes til fremstilling av umettede polyesterharpikser og som frostvæske.
I tillegg anvendes propylenoksyd ved fremstilling av propylenglykoleter. Denne eteren har søknad i produksjon av maling, klær, blekk, harpiks og rengjøringsmidler.
Til syntese av alkoholer og andre anvendelser
Propylen tillater oppnåelse av noen alkoholer, blant annet isopropanol, brukt som løsemiddel i kosmetikk og personlig pleieprodukter. I tillegg oppfyller det funksjonen til antiseptisk middel.
- Isopropanol er involvert i produksjon av maling, harpiks, blekk og limbånd. Det brukes også i farmasøytisk industri.
- Okso-alkohol-2-etylheksanol brukes til fremstilling av ftalater, myknere, klebemidler og malinger.
- Butanol brukes til fremstilling av maling, belegg, harpiks, fargestoffer, legemidler og polymerer.
På den annen side produseres cumen fra kombinasjonen av propylen og benzen. Cumen er hovedforbindelsen ved fremstilling av fenol og aceton, brukt i en rekke produkter, for eksempel polykarbonater, fenolharpikser, epoksyharpikser og metylmetakrylat..
Endelig brukes akrylsyre - et annet produkt avledet fra propylen - til fremstilling av akrylestere og harpikser for maling, belegg og klebemiddel..
referanser
- Michal Osmenda (26. desember 2007). Lys brannen min. [Figur]. Hentet 23. mai 2018, fra: commons.wikimedia.org
- Linde-gruppen. (2018). Propylen. Hentet 23. mai 2018, fra: linde-gas.com
- Wikipedia. (2018). Propen. Hentet 23. mai 2018, fra: en.wikipedia.org
- Pubchem. (2018). Propylen. Hentet 27. mai 2018, fra: pubchem.ncbi.nlm.nih.gov
- Vesovic Velisa. (7. februar 2011). Propylen. Hentet 27. mai 2018, fra: thermopedia.com
- Jeffrey S. Plotkin. (8. august 2016). Propylenkvanta. Hentet 27. mai 2018, fra: acs.org
- ICI. (6. november 2017). Propylenbruk og markedsdata. Hentet 27. mai 2018, fra: icis.com


