Ammoniumsulfat Kjemisk struktur, egenskaper og bruksområder
den ammoniumsulfat Det er et ternært og ammoniakkalt uorganisk salt av svovelsyre. Dens kjemiske formel er (NH4)2SW4. Derfor sier de støkiometriske proporsjonene at for hver sulfatanion er det to ammoniumkationer som interagerer med det. Dette tillater saltets nøytralitet ((+1) ∙ 2 + (-2)).
Nomenklaturen skyldes det faktum at det er et salt avledet fra H2SW4, endre suffikset "uric" til "ato". Dermed erstattes de to første protonene med NH4+, reaksjonsprodukt med ammoniakk (NH3). Deretter er den kjemiske ligningen for dens syntese: 2 NH3 + H2SW4 => (NH4)2SW4
Ammoniumsulfat er en nitrogen- og svovelbutikk, både uunnværlig i jordens og gjødselens kjemi.
index
- 1 Kjemisk struktur
- 2 Fysiske og kjemiske egenskaper
- 2,1 Molekylvekt
- 2.2 Fysisk utseende
- 2.3 lukt
- 2.4 Smeltepunkt
- 2,5 Løselighet
- 2,6 tetthet
- 2,7 Damptrykk
- 2,8 flammepunkt
- 2,9 pH
- 2,10 Stabilitet
- 2.11 Nedbrytning
- 2.12 Korrosjon
- 3 bruksområder
- 3.1 I landbruket
- 3.2 Som et analytisk reagens
- 3.3 Ved utfelling og isolering av proteiner
- 3.4 I bransjen
- 3.5 Andre anvendelser
- 4 referanser
Kjemisk struktur
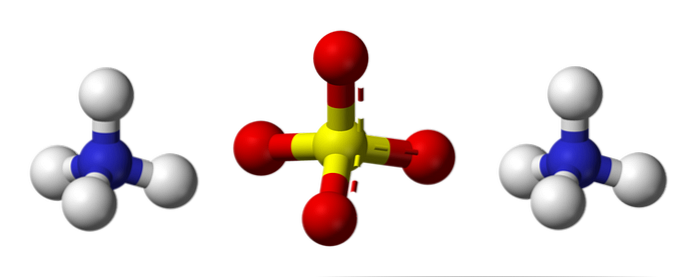
Det øvre bildet illustrerer molekylære geometrier av NH-ioner4+ og så42-. De røde kulene samsvarer med oksygenatomene, de hvite kulene tilsvarer hydrogenatomer, de blå kulene til nitrogenatomet og de gule kulene samsvarer med svovelatomet.
Begge ioner kan betraktes som to tetraederer, og har således tre enheter som samvirker for å danne et orthorhombisk krystallarrangement. Sulfatanionen er SO42- og kan donere eller godta fire hydrogenbindinger, akkurat som NH-kation4+.
Fysiske og kjemiske egenskaper
Molekylvekt
132,134 g / mol.
Fysisk utseende
Solid hvit. Orthorhombic hvite eller brune krystaller, avhengig av urenhetsnivåer.
lukt
toalett.
Smeltepunkt
280 ºC. Dette smeltepunkt, lav sammenlignet med andre ioniske forbindelser, er at det er et salt med monovalente kationer (+1) og ulike ioner i deres størrelser, slik at fast materiale med en lav krystallgitter energi.
løselighet
76,4 g / 100 g vann ved 25 ºC. Denne affiniteten for vann skyldes den store kapasiteten av dets molekyler til å solvatere ammoniumioner. På den annen side er det uoppløselig i aceton og i alkohol; det vil si i løsningsmidler mindre polare enn vann.
tetthet
1,77 g / cm3 ved 25 ºC.
Damptrykk
1,871 kPa ved 20 ºC.
Brennbarhetspunkt
26 ºC.
pH-
5,0-6,0 (25 ° C, 1 M oppløsning). Den litt sure pH skyldes hydrolysen av NH4+ i vann, produserer H3O+ ved lave konsentrasjoner.
stabilitet
Stabil i egnede miljøforhold. Ved kontakt med sterke oksidanter kan det ta ild.
nedbrytning
Det begynner å dekomponere ved 150 ºC, og frigjør giftige damper av svoveloksyd, nitrogenoksid og ammonium.
korrosjon
Angriper ikke jern eller aluminium.
søknader

I landbruket
- Ammoniumsulfat brukes som gjødsel i alkaliske jordarter. Ammoniumsaltet har 21% nitrogen og 24% svovel i sammensetningen. Imidlertid er det forbindelser som gir en større mengde nitrogen enn ammoniumsulfat; Fordelen med sistnevnte er dens høye konsentrasjon av svovel.
- Svovel er essensielt i syntese av proteiner, siden flere aminosyrer, som cystin, metionin og cystein, har svovel. Av disse grunnene fortsetter ammoniumsulfat å være en av de viktigste gjødselene.
- Den brukes i avlinger av hvete, mais, ris, bomull, poteter, hamp og frukttrær.
- Lav pH av alkaliske jordarter på grunn av deres bidrag til nitrifiseringsprosessen utført av mikrober. Ammonium (NH) brukes4+) for å produsere nitrat (NO3-) og slipp H+: 2NH4+ + 4O2 => 2NO3- + 2H2O + 4H+. Økningen i hydrogenkonsentrasjonen reduserer pH i alkaliske jordarter og tillater mer bruk.
- I tillegg til sin anvendelse som gjødsel, det ammoniumsulfat som et adjuvans virker løselige insekticider, herbicider og fungicider, som sprøytes på avlinger.
- Sulfat er i stand til å sekvestrere ioner som finnes i jord og i vanningsvannet som er nødvendige for livet til visse patogener. Blant de ioner som ammoniumsulfatet fanger er Ca2+, Mg2+, troen2+ og troen3+. Denne tiltak forsterker den mikrobicide effekten av de nevnte midler.
Som et analytisk reagens
Ammoniumsulfat virker som et utfellingsmiddel i elektrokjemisk analyse, i mikrobiologiske kulturmedier og i fremstillingen av ammoniumsalter.
Ved utfelling og isolering av proteiner
Ammoniumsulfat brukes i isolering og rensing av proteiner, spesielt plasmaproteiner. En mengde ammoniumsulfat tilsettes til plasmaet til en viss konsentrasjon; Dermed utsettes utfelling av en gruppe proteiner.
Bunnfallet oppsamles ved sentrifugering og ytterligere mengde ammoniumsulfat tilsettes supernatanten, og ved en ny konsentrasjon oppstår utfelling av en annen gruppe proteiner..
Gjentakelsen av den foregående prosessen i sekvensiell form tillater oppnåelse av forskjellige fraksjoner av plasmaproteiner som et resultat.
Før den nye teknologien for molekylærbiologi ble vist, tillot denne prosedyren isolering av plasmaproteiner av stor betydning i medisin, for eksempel: immunoglobuliner, koagulasjonsfaktorer, etc..
I bransjen
Ammoniumsulfat virker for å forsinke starten av brannen i tekstilindustrien. Det brukes som tilsetningsstoff i elektroplateringsindustrien. Det brukes også i produksjon av hydrogenperoksid, ammoniumklorid, etc..
Andre bruksområder
- Ammoniumsulfat brukes som et reguleringsmiddel for osmotisk trykk og som et saltfellingmiddel.
- I form av ammoniumlaurylsulfat reduseres overflatespenningen av vannet, slik at det blir mulig å separere forurensninger ved å øke vannets hardhet.
- Det er et korrosjonsmiddel.
- Det brukes som et tilsetningsstoff som regulerer surhet i meldeg og brød.
referanser
- OECD SIDS. (Oktober 2004). Ammoniumsulfat. [PDF]. Hentet 27. april 2018, fra: inchem.org
- The Mosaic Company. (2018). Ammoniumsulfat. Hentet 27. april 2018, fra: cropnutrition.com
- Wikipedia. (2018). Ammoniumsulfat. Hentet 27. april 2018, fra: en.wikipedia.org
- Pubchem. (2018). Ammoniumsulfat. Hentet 27. april 2018, fra: pubchem.ncbi.nlm.nih.gov UpSticksNGo Crew.
- (23. juli 2015). [Figur]. Hentet 27. april 2018, fra: flickr.com
- Paula Papp (22. februar 2017). Ammoniumsulfatapplikasjoner og anvendelser. Hentet 27. april 2018, fra: business.com


