Proteinase K egenskaper, enzymatisk aktivitet og applikasjoner
den proteinase K er et enzym som tilhører gruppen av serinproteaser, det vil si at den har sitt aktive katalytiske senter en aminosyre serin og har funksjonen til å bryte peptidbindingene ved hydrolyse. Dette enzymet tilhører i sin tur familien av proteiner subtilisiner (peptidase S8).
Proteinase K har en molekylvekt (MW) på 28 900 dalton og ble isolert for første gang i 1974 fra ekstrakter av sopp Engyodontium album, tidligere kjent av navnet på Tritirachium-album Limber.
Det presenterer en høy proteolytisk kapasitet, demonstrert for å kunne nedbryte keratin tilstede i håret. Ordet keratin på engelsk er skrevet "keratin", derfor har det blitt kalt "proteinase K".
På grunn av sin høye kapasitet til å spalte native proteiner, er dette enzymet nyttig i forskjellige molekylærbiologi teknikker. Det er hovedsakelig brukt til å isolere og forberede nukleinsyrer med høy molekylvekt (MW).
Proteinase K virker ved å frigjøre det nukleære DNA, mens ødeleggelsen av proteiner og inaktiverer RNaser og DNaser, det vil si eliminerer nukleasene i DNA- og RNA-preparatene..
På den annen side har det blitt sett at proteinase K kan hydrolysere noen denaturerte, nasjonale proteiner som har vekket interesse for forskere for bruk i studien av prionproteiner (PrPC).
Imidlertid, til tross for sin høye potens eksistere proteolytiske proteiner som er resistente overfor virkningen av proteinase K. Blant disse unormale proteiner kalt prioner (PrPSc) forbundet med TSE er.
index
- 1 Egenskaper av proteinase K
- 2 Enzymatisk aktivitet
- 3 applikasjoner
- 4 Fordeler med proteinase K
- 5 Proteinase-resistente proteiner K
- 6 Referanser
Egenskaper av proteinase K
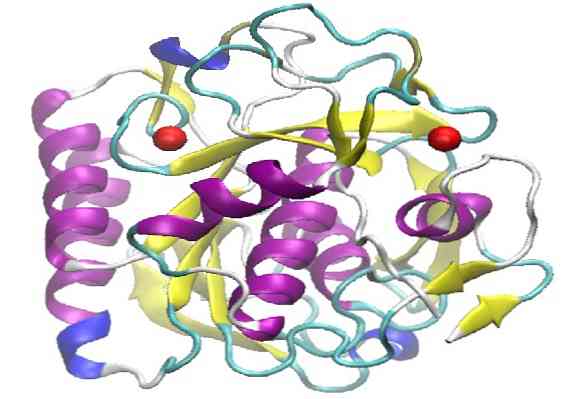
Proteinase K har en tertiær struktur dannet av tre lag, med et p-ark med syv kjeder spaltet mellom to lag av helikser. Fordi den tilhører familien til S8-peptidaser, kjennetegnes den av å ha en katalytisk triad i sitt aktive sted, hvis sekvensielle rekkefølge er (Asp, His og Ser), som skiller dem fra andre familier av peptidaser..
Dette enzymet fra gruppen serinproteaser karakteriseres ved hydrolysering av peptidbindingene nær karboksylgruppen av de alifatiske og aromatiske aminosyrer.
Dessuten er det i stand til å virke i nærvær av visse etsende, slik som natriumdodecylsulfat (SDS), Tris-HCl og EDTA, som brukes til å hjelpe denaturering av proteiner, slik at de mister sine opprinnelige struktur stoffer.
Dette er et foreløpig trinn i fremstillingen av proteiner for elektroforese teknikken. PH-området ved hvilken proteinase K virker, er ganske bred (2,0 til 12,0), med en optimal pH mellom 7,5 og 12,0, og dens isoelektriske punkt er 8,9. Som det kan observeres, er det aktivt mot et meget bredt spekter av pH.
En annen egenskap som skiller seg ut i proteinase K er dens stabilitet i nærvær av høye temperaturer (50-60 ° C).
Enzymatisk aktivitet
Proteinase K trenger tilstedeværelse av kalsiumion, selv om dette ikke påvirker dets aktivitet, dersom det er viktig å opprettholde stabiliteten.
For at proteinase K skal utføre fullstendig fordøyelse av substratet, er det nødvendig med en kontakttid på mellom 5 minutter og 2 timer.
Imidlertid i denne forstand Daza et al. Sammenlignet med renheten av DNA oppnådd ved flere ganger med eksponering for proteinase K, og konkluderte med at en langvarig inkubasjon (opptil 24 timer) signifikant forbedrer DNA-kvaliteten.
Nå, i forhold til konsentrasjonen som brukes av proteinase K-enzymet i de forskjellige protokollene, kan det sies at det er veldig variert.
Den kan brukes fra svært lave konsentrasjoner (5 μg / ml) til konsentrasjoner på 500 μg / ml. Men de hyppigste arbeidskonsentrasjonene varierer mellom 50-100μg / ml, spesielt for proteinfordeling og nukleaseinaktivering. Selv om en konsentrasjon på 2 mg / ml er nødvendig for vevsbehandling.
søknader
Dens applikasjoner er svært brede og kan oppsummeres i følgende:
-Den brukes i fordøyelsen av proteiner og DNA-ekstraksjonsmetoder som er flere: utsalting, PK-SDS, cetyltrimetylammoniumbromid-ammoniumbromid (CTAB), og kaliumacetat modifisert ekstraksjon med natriumjodid.
-Inaktivering av nukleaser (RNaser og DNaser).
-I hybridiseringsteknikken in situ (HIS), for å frigjøre nukleinsyren, i tillegg til eliminering av uønskede proteiner.
-Protein modifikasjon.
-På forskningsnivå, i ulike studier.
Fordeler med proteinase K
Flere komparative studier har blitt utført blant DNA-ekstraksjonsteknikker ved bruk av Proteinase K, med andre som ikke bruker det, og alle konkluderer med at det er større fordeler ved bruk av enzymet. Blant fordelene kan følgende nevnes:
-DNA med høy molekylvekt av høy kvalitet og renhet er oppnådd.
-Det ekstraherte DNA er stabilt opptil 3 måneder.
Det ekstraherte DNA kan brukes i følgende teknikker: Southern blot, polymerasekjedereaksjon (PCR), elektroforese, blant andre.
Proteiner resistente mot proteinase K
Forskning har konkludert med at prioner (PrPSc toksisk unormale proteiner) blir differensiert fra PrPC proteiner (native) for å være resistent mot virkningen av proteinase K, mens PrPC er følsomme for virkningen.
Andre forfattere har beskrevet at i strukturen av PrPSc er det sensitive deler og andre resistente mot proteinase K. Imidlertid er begge deler like giftige og smittsomme..
På den annen side isolerte Bastian og samarbeidspartnere i 1987 4 proteiner av 28, 30, 66 og 76 kda fra en art av Spiroplasma mirum. Alle var resistente mot virkningen av proteinase K og hadde også en kryssreaksjon med noen prioner.
Det er kjent at denne arten kan føre til grå stær og signifikante nevrologiske skader og på grunn av vitenskapelige funn Bastian, blant annet forskning, har prøvd å linke til dette mikroorganisme med overførbare spongiforme encefalopatier.
Imidlertid er etiologien til denne degenerative nevrologiske patologien fortsatt tilskrevet prioner i dag.
I denne forbindelse identifiserte Butler og samarbeidspartnere i 1991 og karakteriserte en klasse av 40 Kda proteinase resistent protein K fra to stammer av Mycoplasma hyorinis. Dette patogen påvirker svinene, infiserer vevet, men i dette tilfellet var det ingen kryssreaksjon med de testede prionene.
Mer forskning er nødvendig for å belyse mange ukjente om det.
referanser
- Bastian F, Jennings R og Gardner W. 1987. Antiserum til scrapieassosiert fibrilprotein kryssreagerer med Spiroplasma mirum fibrilproteiner. J. Clin. Microbiol. 25: 2430-2431.
- Daza C, Guillen J, King J, Ruiz V. Evaluering av en DNA-ekstraksjons- og rensemetode fra muskelvev fastgjort i formaldehyd fra uidentifiserte kadavere. Med Magazine, 2014; 22 (1): 42-49,
- Butler G, H Kotani, Kong L, M Frick, Evancho S, Stanbridge E, og McGarrity G. Identifisering og karakterisering av proteinase K-resistente proteiner i Medlemmer av klassen Mollicutes. Infeksjon og immunitet, 1991, 59 (3): 1037-1042
- López M, Rivera M, Viettri M, Lares M, Morocoima A, Herrera L, et al. Sammenligning av to protokoller for ekstrahering av DNA fra Trypanosoma cruzi vokst i aksenisk medium. Rev. Peru. Med. Offentlig helsepersonell 2014; 31 (2): 222-227. Tilgjengelig på: scielo.org
- Jiménez G, Villalobos M, Jiménez E og Palma W. Bestemmelse av effektiviteten av fem DNA-ekstraksjonsprotokoller fra paraffinmateriale for molekylære studier. Rev Méd Univ Costa Rica. 2007; 1 (1): 10-19.


