Osmolaritetsformel, hvordan å beregne det og forskjell med osmolalitet
den osmolaritet er parameteren som måler konsentrasjonen av en kjemisk forbindelse i en liter løsning, så lenge den bidrar til den kolligative egenskapen kjent som osmotisk trykk av løsningen.
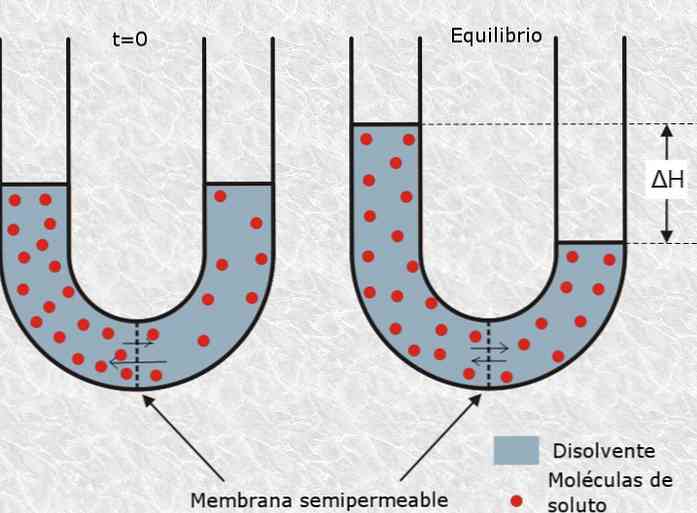
Her er det osmotiske trykk av en oppløsning refererer til mengden av trykk som er nødvendig for å stoppe den osmoseprosessen, som er definert som den selektive passasje av partikler av løsningsmiddel gjennom en semipermeabel eller porøs membran fra en løsning av lavere konsentrasjon til en mer konsentrert.
Også enheten som brukes til å uttrykke mengden av oppløste partikler, er osmol (hvis symbol er Osm), som ikke er en del av det internasjonale system av enheter (SI) som brukes i nesten hele verden. Så konsentrasjonen av løsemiddelet i løsningen er definert i enheter av Osmoles per liter (Osm / l).
index
- 1 formel
- 1.1 Definisjon av variablene i osmolaritetsformelen
- 2 Hvordan beregne det?
- 3 Forskjeller mellom osmolaritet og osmolalitet
- 4 referanser
formel
Som tidligere nevnt uttrykkes osmolaritet (også kjent som osmotisk konsentrasjon) i enheter definert som Osm / l. Dette skyldes forholdet til bestemmelse av osmotisk trykk og måling av løsningsmiddeldiffusjon ved osmose.
I praksis kan den osmotiske konsentrasjonen bestemmes som en fysisk mengde ved bruk av et osmometer.
Det osmometer som er et instrument som brukes ved målingen av det osmotiske trykk av en oppløsning, og bestemmelse av andre sammenbindende egenskaper (som for eksempel damptrykk, øket kokepunkt eller senkning av frysepunktet) for å oppnå verdien av løsningen av osmolariteten.
På denne måten, for å beregne denne måleparameteren, brukes følgende formel, som tar hensyn til alle faktorene som kan påvirke denne egenskapen..
Osmolaritet = ΣφjegnjegCjeg
I denne ligningen er osmolaritet etablert som summen som følge av å multiplisere alle verdiene hentet fra tre forskjellige parametere, som vil bli definert nedenfor.
Definisjon av variablene i osmolaritetsformelen
Først osmotisk koeffisient, representert ved den greske bokstaven φ (phi), som forklarer hvor mye den ideelle løsningen atferd, eller med andre ord, er graden av ikke-ideality som manifesterer det oppløste i løsningen bort.
På den enkleste måten refererer φ til dissosirasjonsgrad for løsemiddelet, som kan ha en verdi mellom null og en, hvor den maksimale verdien av enheten representerer en dissosiasjon på 100%; det er absolutt.
I noen tilfeller - slik som sukrose - overgår denne verdien enhet; mens i andre tilfeller, som for salter, forårsaker påvirkning av elektrostatiske interaksjoner eller krefter en osmotisk koeffisient med en verdi mindre enn enhet, selv om absolutt dissosiasjon oppstår.
På den annen side angir verdien av n mengden partikler hvor et molekyl kan dissosieres. For ioniske arter er natriumklorid (NaCl), hvis verdi på n er lik to, gitt som et eksempel; mens i det ikke-ioniserte glukosemolekylet er verdien av n lik en.
Endelig representerer verdien av c konsentrasjonen av oppløsningen, uttrykt i molar enheter; og abonnementet jeg refererer til identiteten til et bestemt løsemiddel, men det må være det samme når man multipliserer de tre faktorene nevnt ovenfor og dermed oppnår osmolaritet.
Hvordan beregne det?
I tilfelle av KBr-ionisk forbindelse (kjent som kaliumbromid), hvis vi har en oppløsning med en konsentrasjon på 1 mol / l KBr i vann, følger det at denne har en osmolaritet lik 2 osmol / l.
Dette skyldes sin sterke elektrolyttegn, som favoriserer sin fullstendige dissosiasjon i vann og tillater frigivelse av to uavhengige ioner (K+ og Br-) som har litt elektrisk ladning, slik at hver mol KBr er lik to osmoler i oppløsning.
Analogt, for en løsning med en konsentrasjon lik 1 mol / l BaCl2 (kjent som bariumklorid) i vann, den har en osmolaritet lik 3 osmol / l.
Dette skyldes at tre uavhengige ioner slippes ut: en Ba ion2+ og to Cl ioner-. Deretter ble hver mol BaCl2 tilsvarer tre osmol i oppløsning.
På den annen side gjennomgår ikke-ioniske arter en slik dissosiasjon og oppstår en enkelt osmol for hver mol av løsemiddel. I tilfelle en glukoseoppløsning med en konsentrasjon lik 1 mol / l, er dette lik 1 osmol / l av løsningen.
Forskjeller mellom osmolaritet og osmolalitet
En osmol er definert som antall partikler som oppløses i et volum lik 22,4 liter løsningsmiddel, underkastes en temperatur på 0 ° C, og som forårsaker dannelsen av et osmotisk trykk lik 1 atm. Det skal bemerkes at disse partiklene anses osmotisk aktive.
I denne forstand refererer egenskapene kjent som osmolaritet og osmolalitet til samme måling: konsentrasjonen av løsemiddel i en løsning eller på annen måte, innholdet av totale partikler av løsemiddel i oppløsning.
Den grunnleggende forskjellen som er etablert mellom osmolaritet og osmolalitet er i enhetene der hver enkelt er representert:
Osmolaritet uttrykt i form av mengde av substans pr volum av oppløsning (dvs. osmol / l), mens osmolaliteten er uttrykt i mengde av stoff regnet på vekt av løsningsmiddel (dvs. osmol / kg oppløsning).
I praksis brukes begge parametrene på en likegyldig måte, selv om de manifesterer seg i forskjellige enheter, på grunn av det faktum at det er en uansett forskjell mellom de totale målingene i de forskjellige målingene.
referanser
- Wikipedia. (N.d.). Osmotisk konsentrasjon. Hentet fra es.wikipedia.org
- Chang, R. (2007). Kjemi, niende utgave. Mexico: McGraw-Hill.
- Evans, D. H. (2008). Osmotisk og ionisk regulering: celler og dyr. Hentet fra books.google.co.ve
- Potts, W. T., og Parry, W. (2016). Osmotisk og ionisk regulering i dyr. Hentet fra books.google.co.ve
- Armitage, K. (2012). Undersøkelser i generell biologi. Hentet fra books.google.co.ve


