Sølv sulfid (Ag2S) struktur, egenskaper, nomenklatur, bruk
den sølvsulfid er en uorganisk forbindelse hvis kjemiske formel er Ag2S. Den består av et sortgråt fast stoff dannet av Ag kationer+ og anioner S2- i et forhold på 2: 1. S2- det er veldig lik Ag+, fordi begge er myke ioner og de klarer å stabilisere seg med hverandre.
Sølv ornamenter har en tendens til å mørkne, og mister sin karakteristiske glans. Fargeskiftet er ikke et produkt av oksidasjonen av sølvet, men av dets reaksjon med hydrogensulfidet tilstede i miljøet ved lave konsentrasjoner; Dette kan komme fra rotting eller nedbrytning av planter, dyr eller matvarer som er rike på svovel.

H2S, hvis molekyl bærer et svovelatom, reagerer med sølv i henhold til følgende kjemiske ligning: 2Ag (s) + H2S (g) => Ag2S (s) + H2(G)
Derfor er Ag2S er ansvarlig for de svarte lagene som er dannet på sølv. Men i naturen kan dette svovelet også finnes i acantita og argentita mineraler. De to mineralene skiller seg fra mange andre av deres svarte og lyse krystaller, som for det faste stoffet i det øvre bildet.
The Ag2S presenterer polymorfe strukturer, attraktive elektroniske og optoelektroniske egenskaper, er halvleder og lover å være materiale for utvikling av fotovoltaiske enheter, som solceller.
index
- 1 struktur
- 2 Egenskaper
- 2,1 Molekylvekt
- 2.2 Utseende
- 2.3 lukt
- 2.4 Smeltepunkt
- 2,5 Løselighet
- 2.6 Struktur
- 2,7 brytningsindeks
- 2,8 Dielektrisk konstant
- 2.9 Elektronikk
- 2.10 Reduksjonsreaksjon
- 3 Nomenklatur
- 3.1 Systematikk
- 3,2 lager
- 3.3 Tradisjonell
- 4 bruksområder
- 5 referanser
struktur
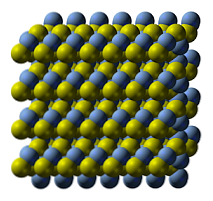
Den krystallinske strukturen av sølvsulfid er illustrert i det øvre bildet. De blå kulene samsvarer med Ag kasjonene+, mens de gule til anionene S2-. The Ag2S er polymorf, noe som betyr at det kan adoptere flere krystallinske systemer under visse temperaturforhold.
Hvordan? Gjennom en faseovergang. Jonene omorganiseres på en slik måte at temperaturøkningen og vibrasjonene av det faste stoffet ikke forstyrrer den elektrostatiske tiltrengnings-avstøtingsvekt. Når dette skjer, sies det at det er en faseovergang, og det faste stoffet viser derfor nye fysiske egenskaper (som glans og farge).
The Ag2S ved normale temperaturer (lavere enn 179ºC), har den en monoklinisk krystallinsk struktur (a-Ag2S). I tillegg til denne faste fase er det andre to: bcc (romsentrert kubisk) mellom 179 til 586ºC, og FCC (kubisk flatesentrert) ved meget høye temperaturer (Ag δ-2S).
Argentittmineralet består av fcc-fasen, også kjent som β-Ag2S. Når de er avkjølt og forvandlet til en klippe, styrker deres strukturelle egenskaper kombinert. Derfor sameksisterer begge krystallstrukturer: monokliniske og bcc. Derfor oppstår svarte faste stoffer med lyse og interessante overtoner.
egenskaper
Molekylvekt
247,80 g / mol
utseende
Gråaktig sorte krystaller
lukt
toalett.
Smeltepunkt
836ºC. Denne verdien er i samsvar med det faktum at Ag2S er en sammensatt med lite ionisk karakter og smelter derfor ved temperaturer under 1000ºC.
løselighet
I vann bare 6,21 ∙ 10-15 g / l ved 25ºC. Det vil si at mengden av det svarte faste stoffet som er oppløst, er ubetydelig. Dette skyldes igjen den lille polare karakteren av Ag-S-bindingen, hvor det ikke er noen signifikant forskjell i elektronegativitet mellom begge atomer.
Også Ag2S er uoppløselig i alle løsningsmidler. Ingen molekyl kan effektivt separere sine krystallinske lag i Ag ioner+ og S2- oppløst.
struktur
Fire lag S-Ag-S-bindinger kan også ses i bildet av strukturen, som beveger seg over hverandre når det faste stoffet blir underlagt forståelse. Denne oppførselen betyr at det til tross for halvleder er duktilt som mange metaller ved romtemperatur.
S-Ag-S-lagene passer ordentlig på grunn av vinkel geometriene som observeres som en zigzag. Å ha en forståelseskraft beveger disse seg på en forflytningsakse og forårsaker dermed nye ikke-kovalente interaksjoner mellom atomer av sølv og svovel.
Brytningsindeks
2.2
Dielektrisk konstant
6
elektronisk
The Ag2S er en amfotert halvleder, det vil si det oppfører seg som om det var av typen n og av typen p. Det er heller ikke sprø, så det har blitt studert for bruk i elektroniske enheter.
Reduksjonsreaksjon
The Ag2S kan reduseres til metallisk sølv ved å bade de svarte stykkene med varmt vann, NaOH, aluminium og salt. Følgende reaksjon finner sted:
3AG2S (s) + 2Al (s) + 3H2O (1) => 6Ag (s) + 3H2S (ac) + Al2O3(S)
nomenklatur
Sølv, hvis elektroniske konfigurasjon er [Kr] 4d105S1, det kan miste bare en elektron: den av sin ytre orbital 5s. Dermed er Ag kation+ forblir med elektronisk konfigurasjon [Kr] 4d10. Derfor har den en unik valens på +1, som bestemmer hvordan forbindelsene skal kalles.
Svovel har på den annen side elektronisk konfigurasjon [Ne] 3s23p4, og det trenger to elektroner for å fullføre sin valensoktett. Når den får disse to elektronene (fra sølv), forvandles den til svovelanionen, S2-, med konfigurasjon [Ar]. Det vil si, det er isoelektronisk å argon edelgass.
Så at Ag2S må kalles i henhold til følgende nomenklaturer:
systematikk
apesulfid disølv. Her ser vi på antall atomer av hvert element og er angitt av prefikset av greske tellere.
Stock
Sølvsulfid. Når du har en unik valens på +1, er den ikke angitt med romerske tall i parentes: sølvsulfid (I); som er feil.
tradisjonelle
Sulfuro argéntico. Siden sølv "virker" med en valens på +1, er suffikset -ico lagt til i navnet Argentum på latin.
søknader
Noen av de nye bruksområder for Ag2S er de følgende:
-Løsningene i deres nanopartikler (med forskjellige størrelser) har antibakteriell aktivitet, er ikke giftige, og kan derfor brukes innen medisin og biologi..
-Deres nanopartikler kan danne det som er kjent som kvantepotter. Disse absorberer og avgir stråling med større intensitet enn mange organiske fluorescerende molekyler, slik at de kan erstatte sistnevnte som biologiske markører.
-Strukturene til a-Ag2S gjør det til å vise slående elektroniske egenskaper som skal brukes som solceller. Det representerer også et utgangspunkt for syntesen av nye termoelektriske materialer og sensorer.
referanser
- Mark Peplow. (17. april 2018). Halvleder sølv sulfid strekker seg som metall. Tatt fra: cen.acs.org
- Samarbeid: Forfattere og redaktører av volum III / 17E-17F-41C () Sølv sulfid (Ag2S) krystallstruktur. I: O. Madelung, U. Rössler, Schulz M. (red) Ikke-tetrahedrally Bonded Elements og Binary Forbindelser I. Landolt-Bornstein - Condensed Matter Gruppe III (numeriske data og funksjonelle sammenhenger i Science and Technology), vol 41C. Springer, Berlin, Heidelberg.
- Wikipedia. (2018). Sølvsulfid. Hentet fra: en.wikipedia.org
- Stanislav I. Sadovnikov & col. (Juli 2016). Ag2S sølvsulfid nanopartikler og kolloide løsninger: Syntese og egenskaper. Hentet fra: sciencedirect.com
- Azo Materials. (2018). Sølvsulfid (Ag2S) Halvledere. Tatt fra: azom.com
- A. Nwofe. (2015). Utsikter og utfordringer av sølvsulfid tynne filmer: En gjennomgang. Divisjon for materialvitenskap og fornybar energi, Institutt for industriell fysikk, Ebonyi State University, Abakaliki, Nigeria.
- UMassAmherst. (2011). Forelesningsdemonstrasjoner: Rengjøring av tarnished sølv. Tatt fra: lecturedemos.chem.umass.edu
- Study. (2018). Hva er Silver Sulfide? - Kjemisk formel og bruk. Hentet fra: study.com


